
设NA为阿伏加德罗常数的值。下列说法正确的是
A.将0.1 molFeCl3溶于1 L水中,所得溶液含Fe3+离子数目为0.1 NA
B.1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA
C.常温、常压下,4.6 g NO2和N2O4混合气体中含有的氧原子数目为0.2NA
D.在高温下,有1 mol Fe与足量的水蒸气反应,转移电子的数目为3NA
 习题精选系列答案
习题精选系列答案科目:高中化学 来源:2015-2016学年安徽省高一上学期第一次月考化学试卷(解析版) 题型:填空题
(1)当O2和CO2的质量之比为1:1时,物质的量之比为 : ,原子总数之比为: , 在同温同压下,密度之比为: ;在三个同温同体积的容器中,分别充入等质量的①H2②CO2③O2三种气体,则容器内压强由大到小的顺序为: ,若将O2和CO2按物质的量之比为2:3混合,则混合气体的平均相对分子质量为: 。
(2)标准状况下,V L某气体(相对分子质量为M)溶解在a L水中(水的密度近似为1 g/mL),所得溶液的密度为ρg/mL,则溶质的质量分数为: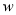 = ,溶质的物质的量浓度:c= mol/L。
= ,溶质的物质的量浓度:c= mol/L。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一上期中测试化学试卷(解析版) 题型:选择题
下列关于物质的量浓度表述正确的是
A.0.2mol·L-1Na2SO4溶液中含有Na+和SO42—总物质的量为0.6mol
B.50mL2mol·L-1NaCl溶液和100mL0.5mol·L-1MgCl2溶液中,Cl-的物质的量浓度相等
C.用1L水吸收22.4L氯化氢所得盐酸的浓度是1mol·L-1
D.10g98%的硫酸(密度为1.84g·cm—3)与10mL18.4mol·L—1的硫酸的浓度是相同的
查看答案和解析>>
科目:高中化学 来源:2016届河南省林州市高三上学期9月质检化学试卷(解析版) 题型:选择题
已知25℃时:①HF(aq)+OH-(aq) F-(aq)+H2O(l) ΔH=-67.7 kJ/mol
F-(aq)+H2O(l) ΔH=-67.7 kJ/mol
②H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol下列有关说法中正确的是
A.HF电离:HF(aq) H+(aq)+F-(aq)△H=+10.4KJ/mol
H+(aq)+F-(aq)△H=+10.4KJ/mol
B.水解消耗0.1 mol F-时,吸收的热量为6.77 kJ
C.中和热均为57.3 kJ/mol
D.含0.1 mol HF、0.1 mol NaOH的两种溶液混合后放出的热量为6.77 kJ
查看答案和解析>>
科目:高中化学 来源:2016届西藏拉萨中学高三上学期第二次月考化学试卷(解析版) 题型:选择题
分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机物有(不含立体异构)
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省四地六校高二上学期10月联考化学试卷(解析版) 题型:填空题
(1)根据如图所示情况,判断下列说法中正确的是 。
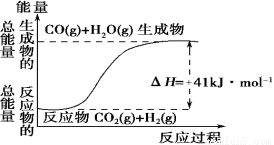
A.其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=41 kJ·mol-1
B.该反应为吸热反应
C.该反应为放热反应
D.若当H2O为液态时反应热为ΔH2,则ΔH2>ΔH
(2)25℃、101 kPa下,已知1g氢气完全燃烧生成液态水时放出142.9 kJ的热量,该反应的热化学方程式是 。
(3)已知反应: N2(g) + O2 (g) = 2NO(g) △H1
2H2(g) + O2(g) = 2H2O(g) △H2
N2(g) + 3H2(g) = 2NH3(g) △H3
利用上述三个反应,计算4NH3(g) + 5O2(g) = 4NO(g) + 6H2O(g) △H4 的反应焓变为 (用含△H1、△H2、△H3的式子表示)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上学期第一次段中考试化学试卷(解析版) 题型:填空题
(1)室温下pH=9的NaOH溶液和pH=9的CH3COONa溶液,设由水电离产生的OH-的物质的量浓度分别为A和B,则A和B的关系为 。
(2)在纯碱溶液中滴入酚酞,溶液变红色,若在该溶液中再滴入过量的BaCl2溶液,所观察到的现象是 ,其原因是 。
(3)对于盐AmBn的溶液:
①若为强酸弱碱盐,其水解的离子方程式是 ;
②若为弱酸强碱盐,其水解的离子方程式是 。
(4)已知KSP (Ag2CrO4)=1.12×10-12,将等体积的4×10-3mo1·L-1的AgNO3和4×10-3mo1·L–1K2CrO4混合,________产生Ag2CrO4沉淀(填“能”或“不能”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期10月月考化学试卷(解析版) 题型:选择题
在恒容密闭容器中,可以作为2NO2(g)  2NO(g)+O2(g) 达到平衡状态的标志是:①单位时间内生成n mol O2的同时生成2n mol NO2;②单位时间内生成n mol O2的同时生成2n mol NO;③混合气体的颜色不再改变;④混合气体的密度不再改变的状态;⑤混合气体的平均相对分子质量不再改变的状态;⑥混合气体中NO与O2的物质的量之比保持恒定;⑦混合气体中NO与NO2的物质的量之比保持恒定
2NO(g)+O2(g) 达到平衡状态的标志是:①单位时间内生成n mol O2的同时生成2n mol NO2;②单位时间内生成n mol O2的同时生成2n mol NO;③混合气体的颜色不再改变;④混合气体的密度不再改变的状态;⑤混合气体的平均相对分子质量不再改变的状态;⑥混合气体中NO与O2的物质的量之比保持恒定;⑦混合气体中NO与NO2的物质的量之比保持恒定
A ①③⑤⑦ B.②④⑤ C.①③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2016届浙江省温州市高三上学期返校联考化学试卷(解析版) 题型:选择题
原子序数依次增大的四种短周期元素X、Y、Z、M。其中Z是金属元素,X的原子半径小于Y ,Y与M同主族,Y的质子数为M的1/2。下列说法一定正确的是
A.X与M的原子序数之差为31
B.Y的离子半径小于Z的离子半径
C.由X与Z组成的化合物,可与水反应放出X2
D.由M与Y组成的化合物,其水化物是强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com