
| A. | H Li Na K | B. | Na Mg Al Cl | C. | I Br Cl F | D. | F O N C |
分析 同一主族元素的第一电离能随着原子序数的增大而减小,同一周期元素的第一电离能随着原子序数的增大而增大,注意同一周期的第ⅡA元素的第一电离能大于第ⅢA族的,第ⅤA族的大于第ⅥA族的.
解答 解:同一主族元素的第一电离能随着原子序数的增大而减小,同一周期元素的第一电离能随着原子序数的增大而增大,注意同一周期的第ⅡA元素的第一电离能大于第ⅢA族的,第ⅤA族的大于第ⅥA族的.
A、H、Li、Na、K属于同一主族元素且原子序数依次增大,其第一电离能随着原子序数的增大而减小,所以其第一电离能依次减小,故A正确;
B、Na、Mg、Al、Cl属于同一周期元素且原子序数依次增大,其第一电离能随着原子序数的增大而增大,但第ⅡA元素的第一电离能大于第ⅢA族的,所以其第一电离能大小顺序为Cl、Mg、Al、Na,故B错误;
C、I、Br、Cl、F属于同一主族元素且原子序数依次减小,同一主族元素的第一电离能随着原子序数的增大而减小,所以I、Br、Cl、F第一电离能依次增大,故C错误;
D、F、O、N、C属于同一周期元素且原子序数依次减小,同一周期元素的第一电离能随着原子序数的增大而增大,但第ⅤA族的大于第ⅥA族的,所以其第一电离能大小顺序是F、N、O、C,故D错误;
故选A.
点评 本题考查了第一电离能大小的判断,难度不大,根据元素周期律来分析解答即可,注意同一周期的第ⅡA元素的第一电离能大于第ⅢA族的,第ⅤA族的大于第ⅥA族的.


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:解答题
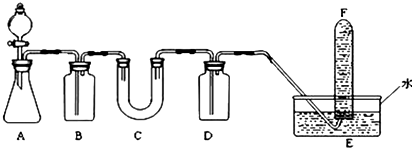
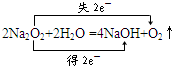 ,所以
,所以查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在熔融电解质中,O2-由正极移向负极 | |
| B. | 电解一共生成0.9 mol气体时,理论上消耗0.1 mol丁烷 | |
| C. | 电解池的阳极反应式为4OH--4e-═2H2O+O2↑ | |
| D. | 通入空气的一极是正极,电极反应式为O2+4e-═2O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 | B. | 8 | C. | 10 | D. | 16 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷分子的比例模型 | B. | 氨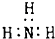 | ||
| C. | Cl-离子的结构示意图 | D. | 8个中子的碳原子的符号${\;}_{6}^{14}$C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
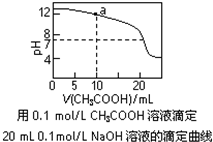
| A. | pH相同的①CH3COONa、②NaHCO3、③Na2CO3三份溶液中的c(Na+):③>②>① | |
| B. | 0.1mol•L-1某二元弱酸强碱盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A) | |
| C. | 图中pH=7时:c(Na+)>c(CH3COO-)>c(OH-)=c(H+) | |
| D. | 图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 46g乙醇中含有的化学键数为7NA | |
| B. | 1mol氯气和足量NaOH溶液反应转移电子数为2NA | |
| C. | 1mol OH- 和1 mol-OH(羟基)中含有的质子数均为9NA | |
| D. | 10L 0.1 mol•L-1 的Na2CO3溶液中,Na+、CO32- 总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 饱和NaCl溶液 | B. | AgNO3 | C. | CuCl2 | D. | 饱和NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化氢在氧气中燃烧 | B. | 二氧化硫通入石灰水中 | ||
| C. | 铁在硫蒸气中燃烧 | D. | 硫酸中加入铁粉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com