
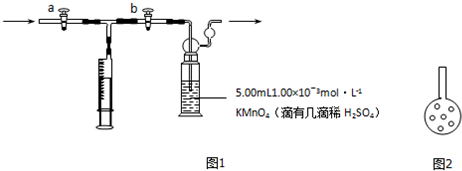
分析 [实验步骤]
(2)打开a关闭b收集室内空气,然后关闭a打开b将橡皮囊中的气体压缩到酸性高锰酸钾溶液中;
[交流讨论]
(1)从实验各个环节可能出现的问题分析;
(2)①根据反应物的接触面积越大,反应越充分来回答;
②通过测定洗气瓶中KMnO4的剩余量,可以得到参加反应的高锰酸钾的量,根据反应可以计算甲醛的量;
(3)根据恰好反应进行完,酸性KMnO4溶液颜色褪去;根据化学方程式4MnO4-+5HCHO+12H+=4Mn2++5CO2↑+11H2O求出HCHO的物质的量,然后求出其体积,最后求出甲醛的浓度.
解答 解:【实验步骤】打开a关闭b收集室内空气,然后关闭a打开b将橡皮囊中的气体压缩到酸性高锰酸钾溶液中,故答案为:a;
【交流讨论】
(1)从实验各个环节可能出现的问题分析,如:未把橡皮囊中气体完全压出、压送气体速度过快、装置气密性较差、导气管伸入KMnO4溶液中太浅、同一地点取样次数太多等,
故答案为:注射器压送气体速度过快、装置气密性较差;导气管伸入KMnO4溶液中太浅、同一地点取样次数太多;
(2)①将插入KMnO4溶液的管子下端改成具有多孔的球泡,反应物的接触面积越大,反应越充分,则测量越准确,有利于提高实验的准确度.
故答案为:可增大气体与溶液的接触面积,使空气中的HCHO被充分吸收;
②通过测定洗气瓶中KMnO4的剩余量,可以得到参加反应的高锰酸钾的量,根据反应可以计算甲醛的量,这样可大大减少抽气的次数,也可达到实验目的,
故答案为:是;
(3)抽气250次,则会抽到空气体积是100mL×250=25000mL=25L,根据反应,设:抽得的气体中含有甲醛的物质的量是n,则
4MnO4-+5HCHO+12H+═4Mn2++5CO2+11H2O,
4 5
0.025L×1.00×10-3mol•L-1 n
解得n=$\frac{5×0.025L×1.00×1{0}^{-3}mol/L}{4}$=3.125×10-6mol,
质量是3.125×10-6mol×30g/mol=9.375×10-5g,
该居室内空气中甲醛的浓度为$\frac{9.375×1{0}^{-5}×1{0}^{3}mg}{25L}$=3.75×10-3mg/L,该居室内空气中甲醛含量超过我国规定,
故答案为:3.75×10-3.
点评 本题主要考查了甲醛的性质、含量的测定原理等知识,题目难度较大,知识点较多.


科目:高中化学 来源: 题型:解答题
 燃料电池是一种高效、环境友好的供电装置,如图是甲烷燃料电池原理示意图.按要求完成下列问题:
燃料电池是一种高效、环境友好的供电装置,如图是甲烷燃料电池原理示意图.按要求完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色化学是指利用化学原理对已产生的环境污染进行治理 | |
| B. | 视频《苍穹之下》再次引起公众对“PM2.5”的关注.“PM2.5”是指大气中直径小于或等于2.5×10-6m的细小颗粒物,这些颗粒扩散在空气中形成胶体 | |
| C. | 离子键、共价键和氢键等化学键都可能对物质的熔沸点产生影响 | |
| D. | 高分子膜在分离提纯、物质制备以及能量转化等领域都有广泛应用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
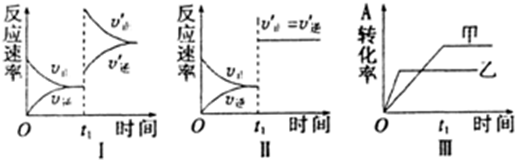
| A. | ①② | B. | ②③ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+,NH4+,SCN-,Cl- | B. | Na+,Cl-,NO3-,SO42- | ||
| C. | Fe2+,Cl-,Na+,NO3- | D. | Fe2+,NH4+,Cl-,OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
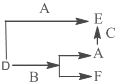 A、B、C分别是三种常见的金属或非金属的单质;D、E、F则是常见的三种氧化物,且有如下所示的转化关系.下列说法中错误的是( )
A、B、C分别是三种常见的金属或非金属的单质;D、E、F则是常见的三种氧化物,且有如下所示的转化关系.下列说法中错误的是( )| A. | D、E中一定都含有A元素 | B. | 单质B肯定是氧化剂 | ||
| C. | A、B、C中一定有一种是O2 | D. | 若A是非金属,则B一定为金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生物质能来源于植物机体加工产品所贮存的能量,绿色植物通过光合作用将化学能转化为生物质能 | |
| B. | 铝硅酸盐分子筛可用于物质分离,还可用作干燥剂、催化剂及催化剂载体 | |
| C. | 人体从食物中摄取蛋白质,在体内先水解成各种氨基酸,经过不断的分解,最终生成水和二氧化碳排出体外 | |
| D. | 铁盐会水解产生具有吸附性的胶体粒子,可用于饮用水的杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量浓度的下列溶液:①H2CO3 ②Na2CO3 ③NaHCO3 ④(NH4)2CO3其中c(CO32-)的大小关系为:②>④>③>① | |
| B. | pH=2的H2C2O4溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)=c(OH-)+c( HC2O4-)+c( C2O42-) | |
| C. | 向0.2 mol•L-1NaHCO3溶液中加入等体积0.1 mol•L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,同浓度的CH3COONa与CH3COOH溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH-)>c(Na+)+c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com