
某硫酸厂以含有SO2的尾气、氨水等为原料,合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质。合成路线如下:
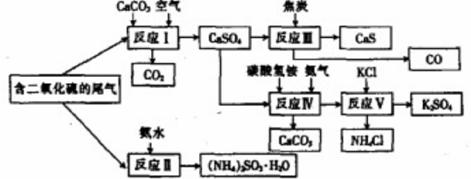
(1)写出反应Ⅲ的化学方程式:
(2)下列有关说法正确的是 (填字母)。
A反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅱ和反应Ⅲ的基本反应类型相同
C.反应Ⅳ需控制在60-70℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
(3) (NH4 )2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统。写出二氧化氮与亚硫酸铵反应的化学方程式: .
(4)很多硫酸厂为回收利用SO2,直接用氨水吸收法处理尾气.
①用15. 0mL 2.0mol·L-1氨水吸收标准状况下448 mL SO2,吸收液中的溶质为
②某同学用酸性KMnO4溶液滴定上述吸收液,当达到滴定终点时,消耗KMnO4溶液25. 00 mL,则酸性KMnO4溶液中,c(KMnO4)=
(5)氨气用途广泛,可以直接用于燃料电池,右图是用氨水作燃料的燃料电池的工作原理。

氨气燃料电池的电解质溶液最好选择 (填“酸性”“碱性”或“中性”)溶液,氮气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池总反应的化学方程式
是_______________________________,负极的电极反应式是_______________________________
【知识点】二氧化硫的性质及物质的制备 化学电源 D3 F3
【答案解析】(1)CaSO4+4C 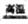 CaS+4CO
CaS+4CO (2分)
(2分)
(2)ACD(2分)
(3)4(NH4)2SO3+2NO2=4(NH4)2SO4+ N2(2分)
(4)①(NH4)2SO3、NH4H SO3
②0.32mol·L-1(各2分)
(5)碱性(1分);4NH3+3 O2=2N2+6H2O(2分);2NH3-6e-+6OH-= N2+6H2O(2分)
解析:(1)碳酸钙、二氧化硫和氧气反应生成硫酸钙和二氧化碳,方程式为2CaCO3+2SO2+O2═2CaSO4+2CO2
(2)A.过量的空气把亚硫酸钙氧化为硫酸钙,故正确;
B.反应Ⅲ化学方程式为:CaSO4+4C=CaS+4CO↑,是氧化还原反应,反应Ⅱ是非氧化还原反应,故错误;
C.防止碳酸氢铵在温度过高时分解得不到需要的目标产物,故正确;
D、氯化铵含N元素,是一种氮肥,故正确;
(3)(NH4)2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统,二氧化氮与亚硫酸铵反应,二氧化氮具有强氧化性能氧化亚硫酸铵,反应生成硫酸铵,本身被还原为氮气,由原子守恒可知化学方程式为4(NH4)2SO3+2NO2=4(NH4)2SO4+N2,
(4)①15. 0mL 2.0mol·L-1氨水的物质的量为0.03mol,吸收标准状况下448 mL SO2,SO2的物质的量为0.02mol,发生反应的方程式为:
3NH3.H2O+2SO2=(NH4)2SO3+NH4H SO3+H2O。
②根据上面的方程式知所得溶液中(NH4)2SO3和NH4H SO3物质的量和为0.02mol,与KMnO4溶液转移电子相等:0.02×2=0.025×c(KMnO4)×5,解得c(KMnO4)=0.32mol·L-1。
(5)氨气燃料电池的电解质溶液最好选择碱性溶液,氮气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池总反应的化学方程式:4NH3+3 O2=2N2+6H2O,
负极发生失电子的氧化反应反应:2NH3-6e-+6OH-= N2+6H2O
【思路点拨】本题考查了二氧化硫的性质及物质的制备,把握题中的信息及发生的反应为解答的关键,侧重二氧化硫的还原性及学生分析能力的考查,难度中等.


科目:高中化学 来源: 题型:
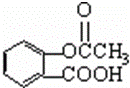
下列关于阿司匹林的说法不正确的是( )
|
| A. | 阿司匹林属于羧酸类有机物 |
|
| B. | 阿司匹林有解热镇痛的作用 |
|
| C. | 服用阿司匹林可能出现胃肠道的不良反应 |
|
| D. | 阿司匹林不能水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
拟用如图所示装置制取下表中四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热,a、b、c、d表示相应仪器中加入的试剂)。
| 气体 | a | b | c | d |
| CO2 | 稀盐酸 | CaCO3 | 饱和NaHCO3溶液 | 浓硫酸 |
| Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓硫酸 |
| NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 氢氧化钠 |
| NO | 稀硝酸 | 铜屑 | H2O | P2O5 |
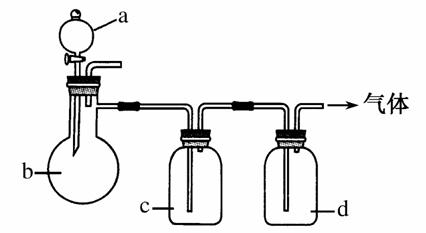
(1)上述方法中可以得到干燥、纯净的________气体。
(2)指出不能用上述方法制取的气体,并说明理由(可以不填满)。
①气体________,理由:______________________________。
②气体________,理由:______________________________。
③气体________,理由:______________________________。
④气体________,理由:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
工厂排放的SO2烟气对环境造成污染,某企业用下列流程综合处理,下列有关说法正确的是( )
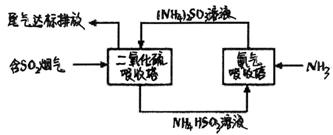
A.二氧化硫吸收塔中发生的反应为:SO2+ SO32-+H2O=2HSO3-
B.氨气吸收塔中发生的反应为:HSO3-+OH-= H2O+ SO32-
C.上述流程利用的是氧化还原反应原理
D.上述流程可循环利用的物质有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质与应用相对应的是 ( )
A.二氧化锰具有强氧化性,可用作H2O2分解的氧化剂
B.K2FeO4具有还原性,可用于自来水的杀菌消毒
C.浓硝酸在常温下能使铝钝化,可用铝槽车运输浓硝酸
D.SO2具有漂白性,能使紫色KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
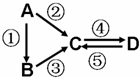
(1)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出该反应的化学方程式:______________________________。
(2)若D物质具有两性,②、③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置:__________________。
(3)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式:__________________________________。
(4)若A是应用最广泛的金属。④反应用到A,②、⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式:__________________________。
(5)若A为淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质. B与C可反应生成A。请写出B的电子式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学在生产和生活中有着重要的应用,下列说法正确的是( )
A.“雾霾天气”、“温室效应”、“光化学烟雾”的形成都与氮氧化物有关
B.“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料
C.白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去
D.能够改善食品的色、香、味,并有防腐、保鲜作用的食品添加剂,须限量使用
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用化学平衡移动原理解释的是( )
A.光照新制的氯水时,溶液的pH逐渐减小
B.加催化剂,使N2和H2在一定条件下转化为NH3
C.可用浓氨水和氢氧化钠固体快速制取氨气
D.增大压强,有利于SO2与O2反应生成SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
已知酸性大小顺序是羧酸>碳酸>酚。下列含溴化合物中的溴原子,在适当条件下都能被羟基(—OH)取代(均可称为水解反应),所得产物能跟NaHCO3溶液反应的是( )
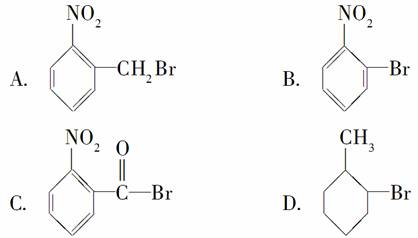
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com