
 一定条件下,Cu2+、Mn2+、Fe3+的浓度对乙酸在光照下催化降解速率的影响如图所示.下列判断不正确的是( )
一定条件下,Cu2+、Mn2+、Fe3+的浓度对乙酸在光照下催化降解速率的影响如图所示.下列判断不正确的是( )| A、Cu2+、Mn2+提高乙酸降解速率的最佳浓度为0.1 mol?L-l |
| B、Fe3+不能提高乙酸降解速率 |
| C、相同条件下,乙酸在Cu2+、Mn2+、Fe3+作用下的降解速率依次减小 |
| D、该实验方案的缺陷之一是未做空白对照实验 |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A |
| 3 |
| 3A |
| 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| X Y Z |
0.1g | 0.3g | 0.5g |
| 1.5% | 223g | 67s | 56s |
| 3.0% | 308s | 109s | 98s |
| 4.5% | 395s | 149s | 116s |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42++2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O |
| B、氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
| C、苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
| D、硝酸亚铁溶液和稀盐酸混合:Fe2++4H++NO3-=Fe3++2H2O+NO↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
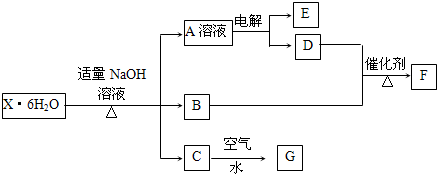
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应中硫酸只表现酸性 |
| B、刺激性气味的气体是氨气 |
| C、红色固体是金属铜 |
| D、1 mol NH4CuSO3完全反应时转移0.5 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L 0.5 mol/L CH3COONa溶液中含有的CH3COO-个数为0.5 NA | ||
| B、6.2g白磷P4中所含的P-P键的个数为0.3 NA | ||
C、在标准状况下,V L CH2O中含有的氧原子个数为
| ||
| D、常温常压下,22g氧气和26g臭氧所含氧原子总数为3 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com