
ĻĀĮŠ»ÆŗĻĪļµÄĖ׳ĘÓė»ÆѧŹ½²»¶ŌÓ¦µÄŹĒ
A£®ĀĢ·Æ£FeSO4”¤7H2O B£®Ć¢Ļõ£Na2SO4”¤10H2O
C£®Ć÷·Æ£Al2(SO4)3”¤12H2O D£®µØ·Æ£CuSO4”¤5H2O

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”øßŅ»ÉĻѧʌµŚ¶ž“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚ¼×”¢ŅŅĮ½ÉÕ±ČÜŅŗÖŠ£¬·Ö±šŗ¬ÓŠ“óĮæµÄCu2+”¢ K+”¢ H+”¢ Cl-”¢ CO32-”¢OH- ĮłÖÖĄė×ÓÖŠµÄČżÖÖ£¬ŅŃÖŖ¼×ÉÕ±µÄČÜŅŗ³ŹĄ¶É«£¬ŌņŅŅÉÕ±µÄČÜŅŗÖŠ“óĮæ“ęŌŚµÄĄė×ÓŹĒ
A£®Cu2+”¢H+”¢Cl- B£®Cl-”¢CO32-”¢OH- C£®K+”¢H+”¢ Cl- D£®K+”¢CO32-”¢OH-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ¹ć¶«Ź”ø߶žÉĻµŚČż“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ¹ż³ĢĪüŹÕČČĮæµÄŹĒ
A£®ĘūÓĶČ¼ÉÕ B£®°±ĘųŅŗ»Æ C£®Ģ¼ĖįøĘ·Ö½ā D£®ÅØĮņĖįĻ”ŹĶ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģøŹĖąŹ”øßČżÉĻµŚČż“ĪÄ£Äāæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĶ¼Ź¾¹ŲĻµÖŠ²»ÕżČ·µÄŹĒ
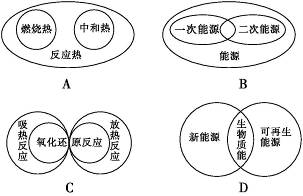
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģøŹĖąŹ”ÕÅŅ“ŹŠøßČżÉĻµŚŅ»“ĪÕļ¶Ļæ¼ŹŌĄķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ĄūÓĆN2ŗĶH2æÉŅŌŹµĻÖNH3µÄ¹¤ŅµŗĻ³É£¬¶ų°±ÓÖæÉŅŌ½ųŅ»²½ÖʱøĻõĖį£¬ŌŚ¹¤ŅµÉĻŅ»°ćæɽųŠŠĮ¬ŠųµŲÉś²ś”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŅŃÖŖ£ŗN2(g)+O2(g) =2NO(g) ”÷H=+180.5kJ/mol
N2(g)+3H2(g)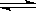 2NH3(g) ”÷H=£92.4kJ/mol
2NH3(g) ”÷H=£92.4kJ/mol
2H2(g)+O2(g)=2H2O(g) ”÷H=£483.6kJ/mol
ŌņNH3“ß»ÆŃõ»ÆÉś³ÉNOŗĶH2O(g)µÄČČ»Æѧ·“Ó¦·½³ĢŹ½æɱķŹ¾ĪŖ£ŗ ”£
£Ø2£©Ä³æĘŃŠŠ”×éŃŠ¾æŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬øıäĘšŹ¼ĒāĘųĪļÖŹµÄĮæ[ÓĆn(H2)±ķŹ¾]¶ŌN2(g)+3H2(g) 2NH3(g)·“Ó¦µÄÓ°Ļģ£¬ŹµŃé½į¹ūæɱķŹ¾³ÉČēÓŅĶ¼ĖłŹ¾µÄ¹ęĀÉ£ØĶ¼ÖŠT±ķŹ¾ĪĀ¶Č£¬n±ķŹ¾ĪļÖŹµÄĮ棩£ŗ
2NH3(g)·“Ó¦µÄÓ°Ļģ£¬ŹµŃé½į¹ūæɱķŹ¾³ÉČēÓŅĶ¼ĖłŹ¾µÄ¹ęĀÉ£ØĶ¼ÖŠT±ķŹ¾ĪĀ¶Č£¬n±ķŹ¾ĪļÖŹµÄĮ棩£ŗ
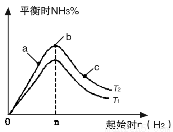
¢Ł±Č½ĻŌŚa”¢b”¢cČżµćĖł“¦µÄĘ½ŗāדĢ¬ÖŠ£¬·“Ó¦ĪļN2µÄ×Ŗ»ÆĀŹ×ī“óµÄŹĒ ”£
¢ŚŌŚĘšŹ¼Ź±ĢåĻµÖŠ¼ÓČėN2µÄĪļÖŹµÄĮæĪŖ1mol”£ČōČŻĘ÷ČŻ»ż
ĪŖ2L£¬n=3mol·“Ó¦“ļµ½Ę½ŗāŹ±H2µÄ×Ŗ»ÆĀŹĪŖ60%£¬Ōņ“ĖĢõ¼žĻĀ£ØT2£©£¬·“Ó¦µÄĘ½ŗā³£ŹżK= ”£
¢ŪĶ¼ĻńÖŠT1ŗĶT2µÄ¹ŲĻµŹĒ£ŗT1 T2”££ØĢī”°>”±”°<”±”°=”±”°ĪŽ·ØČ·¶Ø”±£©
£Ø3£©°±ĘųŗĶŃõĘų“Ó145”ę¾ĶæŖŹ¼·“Ó¦£¬ŌŚ²»Ķ¬ĪĀ¶ČŗĶ“߻ƼĮĢõ¼žĻĀÉś³É²»Ķ¬²śĪļ£ØČēĻĀĶ¼£©£ŗ
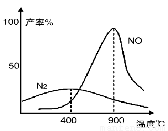
4NH3£«5O2 4NO£«6H2O £»
4NO£«6H2O £»
4NH3£«3O2 2N2£«6H2O
2N2£«6H2O
ĪĀ¶Č½ĻµĶŹ±ŅŌÉś³É ĪŖÖ÷£¬ĪĀ¶ČøßÓŚ900”ꏱ£¬NO²śĀŹĻĀ½µµÄŌŅņ ”£
£Ø4£©N2O5ŹĒŅ»ÖÖŠĀŠĶĻõ»Æ¼Į£¬ĘäŠŌÖŹŗĶÖʱøŹÜµ½ČĖĆĒµÄ¹Ų×¢”£
¢ŁŅ»¶ØĪĀ¶ČĻĀ£¬ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠN2O5æÉ·¢ÉśĻĀĮŠ·“Ó¦£ŗ
2N2O5(g)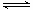 4NO2(g)£«O2(g) ”÷H£¾0£¬ĻĀ±ķĪŖ·“Ó¦ŌŚT1ĪĀ¶ČĻĀµÄ²æ·ÖŹµŃ鏿¾Ż£ŗ
4NO2(g)£«O2(g) ”÷H£¾0£¬ĻĀ±ķĪŖ·“Ó¦ŌŚT1ĪĀ¶ČĻĀµÄ²æ·ÖŹµŃ鏿¾Ż£ŗ
t/s | 0 | 500 | 1000 |
c(N2O5)/mol”¤L”Ŗ1 | 5.00 | 3.52 | 2.48 |
Ōņ500sÄŚNO2µÄÉś³ÉĖŁĀŹæɱķŹ¾ĪŖ____________________”£
¢ŚĻĀĮŠĒéæöÄÜĖµĆ÷øĆ·“Ó¦ŅŃ“ļĘ½ŗāדĢ¬µÄŹĒ ”£
A£®µ„Ī»Ź±¼äÄŚÉś³É2mol NO2µÄĶ¬Ź±ĻūŗÄĮĖlmol N2O5 B£®»ģŗĻĘųĢåµÄŃÕÉ«²»ŌŁ·¢Éś±ä»Æ
C£®»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä D£®ŌŚ¾ųČČŗćČŻµÄČŻĘ÷ÖŠ£¬·“Ó¦µÄĘ½ŗā³£Źż²»ŌŁ±ä»Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”øßŅ»ÉĻ12ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ĻĀĆęČżøö·½·Ø¶¼æÉŅŌÓĆĄ“ÖĘĀČĘų£ŗ
¢Ł4HCl(ÅØ)+MnO2 MnCl2+Cl2”ü+2H2O
MnCl2+Cl2ӟ+2H2O
¢ŚKClO3+6HCl=3Cl2”ü+KCl+3H2O
¢ŪKMnO4+HCl(ÅØ)”ŖKCl+MnCl2+Cl2”ü+H2O(Ī“ÅäĘ½)£¬
øł¾ŻŅŌÉĻČżøö·“Ó¦£¬»Ų“šÓŠ¹ŲĪŹĢā£ŗ
£Ø1£©·“Ó¦µÄ¢ŚµÄĄė×Ó·½³ĢŹ½ĪŖ________________”£
£Ø2£©·“Ó¦¢ŚÖŠ£¬Ńõ»Æ²śĪļÓė»¹Ō²śĪļµÄÖŹĮæ±ČĪŖ____________”£
£Ø3£©Ēė½«·“Ó¦¢ŪÅäĘ½£ŗ__KMnO4+__HCl(ÅØ)=__KClŹ®__MnCl2£«__Cl2”ü+__H2O
£Ø4£©ČōŅŖÖʵĆĻąĶ¬ÖŹĮæµÄĀČĘų£¬¢Ł¢Ś¢Ū·“Ó¦ÖŠµē×Ó×ŖŅʵďżÄæÖ®±ČĪŖ_________”£
£Ø5£©ŅŃÖŖ·“Ó¦¢Ü£ŗ4HCl(g)+O2 2Cl2+2H2O(g)£¬øĆ·“Ó¦Ņ²ÄÜÖʵĆĀČĘų£¬ŌņMnO2”¢O2”¢KMnO4ČżÖÖĪļÖŹŃõ»ÆŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖ________________”£
2Cl2+2H2O(g)£¬øĆ·“Ó¦Ņ²ÄÜÖʵĆĀČĘų£¬ŌņMnO2”¢O2”¢KMnO4ČżÖÖĪļÖŹŃõ»ÆŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖ________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”ø߶žÉĻ12ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŅŃÖŖŌŚ25”ꏱ£¬FeS”¢CuSµÄČܶȻż³£Źż(Ksp)·Ö±šĪŖ6.3”Į10£18”¢1.3”Į10£36.³£ĪĀŹ±ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A£®ĻņH2SµÄ±„ŗĶČÜŅŗÖŠĶØČėÉŁĮæSO2ĘųĢåČÜŅŗµÄĖįŠŌŌöĒæ
B£®½«×ćĮæµÄCuSO4ČܽāŌŚ0.1 mol/LµÄH2SČÜŅŗÖŠ£¬ČÜŅŗÖŠCu2£«µÄ×ī“óÅضČĪŖ1.3”Į10£35 mol/L
C£®ŅņĪŖH2SO4ŹĒĒæĖį£¬ĖłŅŌ·“Ó¦£ŗCuSO4£«H2S===CuS”ż£«H2SO4²»ÄÜ·¢Éś
D£®³żČ„¹¤Ņµ·ĻĖ®ÖŠµÄCu2£«æÉŅŌŃ”ÓĆFeS×÷³Įµķ¼Į
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĞĻÄĢĘįā»ŲĆń֊ѧø߶žÉĻ10ŌĀŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
»ÆŗĻĪļHInŌŚĖ®ČÜŅŗÖŠŅņ“ęŌŚŅŌĻĀµēĄėĘ½ŗā£¬¹ŹæÉÓĆ×÷Ėį¼īÖøŹ¾¼Į£ŗ
HIn (ČÜŅŗ) 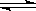 H£«(ČÜŅŗ)£«In£(ČÜŅŗ)
H£«(ČÜŅŗ)£«In£(ČÜŅŗ)
ŗģÉ« »ĘÉ«
ÅضČĪŖ0.02 mol/LµÄĻĀĮŠČÜŅŗ £Ø1£©ŃĪĖį £Ø2£©NaOHČÜŅŗ £Ø3£©NaHSO4ČÜŅŗ £Ø4£©NaHCO3ČÜŅŗ £Ø5£©°±Ė®£¬ĘäÖŠÄÜŹ¹ÖøŹ¾¼ĮĻŌŗģÉ«µÄŹĒ
A£®£Ø1£©£Ø4£©£Ø5£© B£®£Ø2£©£Ø5£© C£®£Ø1£©£Ø3£© D£®£Ø2£©£Ø3£©£Ø5£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016½ģÕć½Ź”Éī»ÆæĪ³ĢøÄøļŠ×÷Š£øßČżÉĻѧʌ11ŌĀĘŚÖŠĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
Ēė»Ų“š£ŗ
£Ø1£©CO2µÄµē×ÓŹ½
£Ø2£©½«Įņ»ÆÄĘČÜŅŗÓėĀČ»ÆĀĮČÜŅŗ»ģŗĻ£¬ÓŠ°×É«³ĮµķŗĶĘųĢåÉś³É£¬µ«“Ė³Įµķ²»ŹĒĮņ»ÆĀĮ”£Š“³öøĆ·“Ó¦µÄĄė×Ó·“Ó¦·½³ĢŹ½£ŗ
£Ø3£©½«NH3Ķعż×ĘČȵÄCuO£¬ÓŠĪŽÉ«ĪŽĪ¶µÄÄŃČÜÓŚĖ®µÄĘųĢåÉś³É£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
£Ø4£©CoCl2³£ÓĆ×÷¶ą²ŹĖ®ÄąµÄĢķ¼Ó¼Į£¬æÉÓĆīܵÄijÖÖŃõ»ÆĪļÓėŃĪĖį·“Ó¦Öʱø(ĘäÖŠCoµÄ»ÆŗĻ¼ŪĪŖ+2”¢+3)”£ĻÖČ”ŹŹĮæÕāÖÖīܵÄŃõ»ÆĪļ£¬æÉÓė480 mL 5 mol”¤L£1 ŃĪĖįĒ”ŗĆĶźČ«·“Ó¦£¬µĆµ½CoCl2ČÜŅŗŗĶ6.72 L»ĘĀĢÉ«ĘųĢå(±ź×¼×“æö)”£ŌņøĆ·“Ó¦µÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ ”£
¢ņĻĀ±ķøų³öĮĖĪåÖÖŌŖĖŲµÄĻą¹ŲŠÅĻ¢£¬ĘäÖŠA”¢B”¢C”¢DĪŖ¶ĢÖÜĘŚŌŖĖŲ”£øł¾ŻŅŌĻĀŠÅĻ¢ĢīæÕ£ŗ
ŌŖĖŲ | Ļą¹ŲŠÅĻ¢ |
A | ŌŚ³£ĪĀ”¢³£Ń¹ĻĀ£¬Ę䵄֏ŹĒĘųĢ壬Ėę×ÅČĖĄą¶Ō»·¾³µÄČĻŹ¶ŗĶŅŖĒóµÄĢįøߣ¬Ėü½«³ÉĪŖ±øŹÜĒąķłµÄĒå½ąČ¼ĮĻ |
B | ¹¤ŅµÉĻĶعż·ÖĄėŅŗĢ¬æÕĘų»ńµĆĘ䵄֏£¬ĘäijÖÖĶ¬ĖŲŅģŠĪĢåŹĒ±£»¤µŲĒņµŲ±ķ»·¾³µÄÖŲŅŖĘĮÕĻ |
C | Ö²ĪļÉś³¤ČżŅŖĖŲÖ®Ņ»£¬ĖüÄÜŠĪ³É¶ąÖÖŃõ»ÆĪļ£¬ĘäÖŠŅ»ÖÖŹĒŌēĘŚŅ½ĮĘÖŠŹ¹ÓƵÄĀé×ķ¼Į |
D | ŹŅĪĀĻĀĘ䵄֏ĪŖµ»ĘÉ«·Ūĩד¹ĢĢ壬¼ÓČČŅ×ČŪ»Æ”£øƵ„ÖŹŌŚŃõĘųÖŠČ¼ÉÕ£¬·¢³öĆ÷ĮĮµÄĄ¶×ĻÉ«»šŃę |
E | ĖüŌŚµŲæĒÖŠ“¢Įæ·įø»£¬ŹĒČĖĢå²»æÉȱɣµÄĪ¢ĮæŌŖĖŲÖ®Ņ»”£Ę䵄֏ĪŖŅų°×É«¹ĢĢ壬ŹĒ¹¤Å©ŅµÉś²śÖŠ²»æÉ»ņȱµÄ½šŹō²ÄĮĻ£¬³£ÓĆÓŚ»śŠµÖʱø”¢½ØÖžµČŠŠŅµ |
£Ø5£© CÓėAŠĪ³ÉµÄijŅ»»ÆŗĻĪļÄÜŗĶCÓėBŠĪ³ÉµÄĮķŅ»ĪŽÉ«»ÆŗĻĪļ(ÕāĮ½ÖÖ»ÆŗĻĪļ·Ö×ÓÖŠŌ×ÓøöŹż±Č½ŌĪŖ1”Ć2)Ņ»ĘšÓĆ×÷»š¼żÖśĶĘ¼Į£¬Į½Õß·¢Éś·“Ӧɜ³ÉĪŽ¶¾ĪļÖŹ£¬Š“³öÉĻŹö»Æѧ·“Ó¦·½³ĢŹ½£ŗ____________”£
£Ø6£©»ÆŗĻĪļXŹĒŌŖĖŲDµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ£¬XŌŚĖ®ÖŠµÄµēĄė·½³ĢĪŖ £»³£ĪĀĻĀ£¬EµÄµ„ÖŹÓė»ÆŗĻĪļX·“Ӧɜ³ÉŃĪY£¬YµÄ»ÆѧŹ½ŹĒ ”£»ÆŗĻĪļZ½öÓÉŌŖĖŲDŗĶE×é³É£¬ Z+ H2O+ O2= X+ Y£¬²śĪļÖŠn(X)£ŗn(Y)=1£ŗ1£¬Š“³ö²¢ÅäĘ½ÉĻŹö·½³ĢŹ½£ŗ ”£
£Ø7£©ŃĪYŹÜĒæČČ»į·¢Éś·Ö½ā·“Ó¦£¬ĘäĘųĢå²śĪļÓÉŌŖĖŲDµÄŃõ»ÆĪļ×é³É£¬ĒėÉč¼ĘŅ»øöæÉŠŠµÄ¶ØŠŌŹµŃ飬ŃéÖ¤ĘäĘųĢå²śĪļÖŠĖłŗ¬ŌŖĖŲDµÄŃõ»ÆĪļµÄ×é³É ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com