
| A. | 溶液中阴离子浓度的大小顺序:c(S2-)>c(OH-)>c(HS-) | |
| B. | c(Na+)=2c(S2-)+c(OH-)+c(HS-) | |
| C. | c(Na+)=c(S2-)+c(HS-) | |
| D. | 向溶液中加入少量NaOH固体,能促进水的电离 |
分析 A.Na2S溶液存在S2-+H2O?HS-+OH-,HS-+H2O?H2S+OH-,第一步水解程度大于第二步水解;
B.从电荷守恒的角度分析;
C.依据元素守恒分析;
D.向溶液中加入少量NaOH固体,抑制水的电离.
解答 解:A.Na2S溶液存在S2-+H2O?HS-+OH-,HS-+H2O?H2S+OH-,则有c(OH-)>c(HS-),一般来说水解程度较小,则应有c(S2-)>c(OH-)>c(HS-),故A正确;
B.溶液存在电荷守恒,应有c(Na+)+c(H+)=2c(S2-)+c(OH-)+c(HS-),故B错误;
C.Na2S中Na元素是S元素个数的2倍,故应有2c(Na+)=c(S2-)+c(HS-)+c(H2S),故C错误;
D.向溶液中加入少量NaOH固体,c(OH-)增大,抑制水的电离,故D错误.
故选A.
点评 本题考查离子浓度大小的比较,题目难度不大,注意从电荷守恒、物料守恒的角度分析,把握盐类水解的原理,易错点为C,注意离子浓度的变化.


科目:高中化学 来源: 题型:解答题
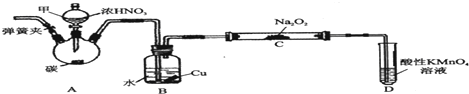

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
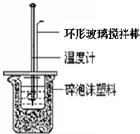 “中和热的测定”实验步骤为:
“中和热的测定”实验步骤为:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(Fe)--溶于足量盐酸,过滤 | B. | KNO3(NaCl)--结晶 | ||
| C. | 水(NaCl)--蒸馏 | D. | CO2(HCl)--氢氧化钠溶液,洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | OH-、H2O、F- | B. | NH3、NH4+、F- | C. | H3O+、NH4+、Cl- | D. | HCl、F2、H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4的摩尔质量是98 | |
| B. | 等质量的O2和O3中所含的氧原子数不同 | |
| C. | 等质量的SO2与SO3中所含硫原子数之比为5:4 | |
| D. | 将98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体可发生丁达尔效应 | B. | 胶体粒子能够发生布朗运动 | ||
| C. | 胶体能透过滤纸但不能透过滤纸 | D. | 胶体粒子直径在1nm-100nm之间 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com