
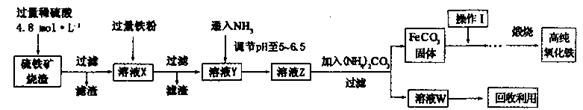


科目:高中化学 来源:不详 题型:填空题
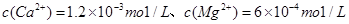 、
、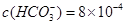
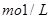 。要软化10 m3这种天然水,需先加入Ca(OH)2 g,再加入Na2CO3 g。
。要软化10 m3这种天然水,需先加入Ca(OH)2 g,再加入Na2CO3 g。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.除去CO中混有的CO2:用氢氧化钠溶液洗气 |
| B.用AlCl3溶液和过量氨水制备Al(OH)3 |
| C.用足量铜粉除去FeCl2溶液中的FeCl3杂质 |
| D.用排水法收集稀HNO3和Cu反应产生的NO气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
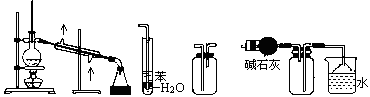
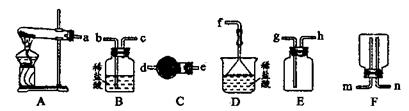
| A.装置①常用于分离互相溶解且沸点相差10℃以上的液态混合物 |
| B.装置②可用于吸收NH3或HCl气体,并防止到吸 |
| C.装置③可用于收集H2、CO2、Cl2、NH3等气体 |
| D.装置④可用于干燥、收集氨气,若将碱石灰改成五氧化二磷,可用于干燥、收集氯化氢 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
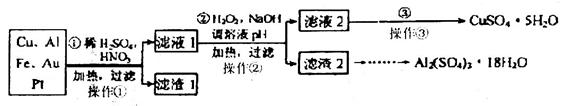
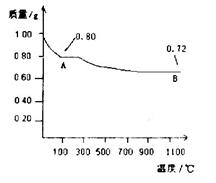
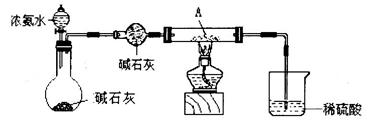
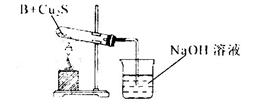
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
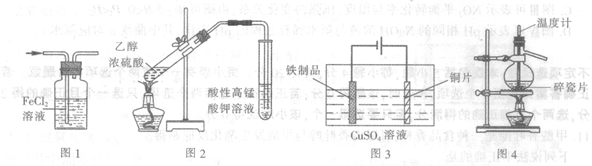
| A.用图1所示装置除去HCl气体中的少量C12 |
| B.用图2所示装置检验加热时产生的乙烯 |
| C.用图3所示装置在铁制品表面镀铜 |
| D.用图4所示装置分离溴的四氯化碳溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.用图1可证明SO2与NaOH溶液发生了反应 |
| B.用图2装置不能证明溴乙烷发生消去反应 |
| C.用图3装置制备Fe( OH)2并能较长时间观察其颜色 |
| D.用图4装置测量Cu与浓硝酸反应产生气体的体积 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
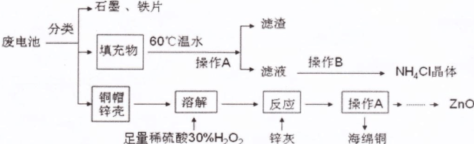
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.可以用溴水来鉴别乙烯和苯 |
| B.可以用金属钠来鉴别乙醇和乙酸 |
| C.可以用新制的氢氧化铜来鉴别葡萄糖和淀粉 |
| D.可以用灼烧的方法来鉴别真丝布料和纯棉布料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com