
| A. | 苯 | B. | 乙基(-CH2CH3) | C. | 碳正离子[(CH3)3C+] | D. | 碳烯(:CH2) |
分析 碳原子最外层电子数为4+共用电子对数+获得电子数(或减去失去电子数).
A.苯中C原子C-H键、大π键;
B.-CH2CH3中CH3中-CH2-中碳原子与碳原子形成1对共用电子对,与氢原子共形成2对共用电子对,含有1个单电子;
C.(CH3)3C+中CH3中碳形成4对共用电子对,满足8电子.中心碳原子与另三个碳原子形成3对共用电子对,且中心碳原子失去一个电子;
D.碳原子与两个氢原子形成2对共用电子对.
解答 解:A.苯中C原子与1个H原子形成1对共用电子对,且与两个C原子成键,苯分子中存在大π键,碳原子都满足最外层为8电子结构,故A正确;
B.-CH2CH3中CH3中碳形成4对共用电子对,满足8电子.-CH2-中碳原子不满足,与碳原子形成1对共用电子对,与氢原子共形成2对共用电子对,含有1个单电子,最外层电子数为4+3=7,故B错误;
C.(CH3)3C+中CH3中碳形成4对共用电子对,满足8电子.中心碳原子与另三个碳原子形成3对共用电子对,且中心碳原子失去一个电子,最外层电子数为4+3-1=6,故C错误;
D.碳原子与两个氢原子形成2对共用电子对,碳原子最外层电子数为4+2=6,故D错误.
故选A.
点评 本题考查8电子结构,难度不大,清楚各微粒结构是解题的关键,注意碳原子最外层电子数为4+共用电子对数+获得电子数(或减去失去电子数).


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 该温度高于25℃ | |
| B. | 由水电离出来的H+的浓度是1.0×10-10 mol•L-1 | |
| C. | 加入NaHSO4晶体抑制了水的电离 | |
| D. | 该温度下加入等体积pH=12的NaOH溶液可使该溶液恰好呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 我国在反兴奋剂问题上的坚决立场是支持“人文奥运”的重要体现.某种兴奋剂的结构如图,关于它的说法正确的是( )
我国在反兴奋剂问题上的坚决立场是支持“人文奥运”的重要体现.某种兴奋剂的结构如图,关于它的说法正确的是( )| A. | 它的化学式为C20H25O3 | |
| B. | 该化合物只能发生取代反应 | |
| C. | 从结构上看,它属于醇类 | |
| D. | 从元素组成上看,它可以在氧气中燃烧生成CO2和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③ | C. | ①⑤⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
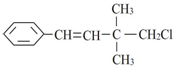 ,关于该有机物,下列叙述不正确的是( )
,关于该有机物,下列叙述不正确的是( )| A. | 所有碳原子不可能在同一平面上 | |
| B. | 属于卤代烃 | |
| C. | 分子式为C12H15Cl | |
| D. | 能发生加成反应、取代反应、加聚反应、消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com