
短周期主族元素X、Y、Z、W原子序数依次增大,X原子最外层有6个电子,Y是至今发现的非金属性最强的元素,Z在周期表中处于周期序数等于族序数的位置,W的单质广泛用作半导体材料。下列叙述正确的是
A.原子最外层电子数由多到少的顺序:Y、X、W、Z
B.原子半径由大到小的顺序:W、Z、Y、X
C.元素非金属性由强到弱的顺序:Z、W、X
D.简单气态氢化物的稳定性由强到弱的顺序:X、Y、W
科目:高中化学 来源:2016届甘肃省天水市高三上学期第三次测试化学试卷(解析版) 题型:选择题
用FeCl3溶液腐蚀印刷电路板上的铜,所得溶液中加入铁粉。对加入铁粉充分反应后的溶液分析合理的是
A.若无固体剩余,则溶液中一定有Fe3+
B.若有固体存在,则溶液中一定有Fe2+
C.若溶液中有Cu2+,则一定没有固体析出
D.若溶液中有Fe2+,则一定有Cu析出
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江哈尔滨六中高一10月月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 某溶液中加入BaCl2溶液,产生不溶于稀盐酸的白色沉淀,则该溶液一定含有SO42﹣
B. FeCl3稀溶液与Fe(OH)3胶体本质区别是分散质粒子的大小
C. Fe(OH)3胶体可以产生电泳现象,由此可知Fe(OH)3胶体带电
D. 用溶解、过滤的方法分离KNO3和NaCl固体的混合物
查看答案和解析>>
科目:高中化学 来源:2016届山东省临沂市高三上学期第一次月考化学试卷(解析版) 题型:选择题
用36.5%的浓盐酸(密度1.2 g·cm-3)配1 mol·L-1的稀盐酸 100 mL,配制过程需用到的仪器组合正确的是
①100 mL量筒;②10 mL量筒;③50 mL 烧杯;④托盘天平;⑤100 mL容量瓶;⑥胶头滴管;⑦玻璃棒
A.①③⑤⑥⑦ B.②③⑦⑤⑥
C.③⑤⑦⑥① D.④③⑦⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
3molA和2.5molB混合于容积为2L的容器内,使它们发生反应2A(s)+3B(g)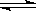 2C(g)+D(g),经过5min生成0.5molD,下列说法正确的是
2C(g)+D(g),经过5min生成0.5molD,下列说法正确的是
A.B的平均消耗速率为0.3mol/(L•min)
B.C的平衡浓度为2mol/L
C.平衡后,增大压强,平衡将向正方向移动
D.若反应容器内气体的密度不再发生变化,说明反应已经达到平衡
查看答案和解析>>
科目:高中化学 来源:2016届浙江省杭州市高三上学期10月月考化学试卷(解析版) 题型:填空题
能源问题是当前人类社会面临的一项重大课题,H2、CO、CH3OH都是重要的能源物质,它们的燃烧热依次为285.8 kJ/mol、282.5 kJ/mol、726.7 kJ/mol。请回答:
(1)已知CO和H2在一定条件下可以合成甲醇:CO+2H2=CH3OH。则H2与CO反应生成CH3OH的热化学方程式为: 。
(2)如图为某种燃料电池的工作原理示意图,a、b均为惰性电极。 ①使用时,空气从 口通入(填“A”或“B”);
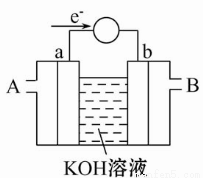
②假设使用的“燃料”是甲醇,a极的电极反应式为:
③假设使用的“燃料”是水煤气(成分为CO、H2)用这种电池电镀铜,待镀金属增重6.4 g,则至少消耗标准状况下水煤气的体积为 。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省杭州市高三上学期10月月考化学试卷(解析版) 题型:选择题
同一短周期的元素W、X、Y、Z的原子序数依次增加,下列叙述正确的是
A.单质的化学活泼性:W<X<Y<Z
B.元素的最高化合价:W<X<Y<Z
C.单质的氧化能力:W<X<Y<Z
D.原子最外层电子数:W<X<Y<Z
查看答案和解析>>
科目:高中化学 来源:2016届浙江省温州市高三上学期期中测试理综化学试卷(解析版) 题型:选择题
五种短周期元素的某些信息如表所示:
元素 | 有关信息 |
X | 最高价氧化物对应的水化物能与其气态氢化物反应生成盐 |
Y | M层上有3个电子 |
Z | 短周期元素中原子半径最大的主族元素 |
W | 其单质是淡黄色固体 |
Q | 最高正价与最低负价代数和为6 |
下列说法正确的是
A.简单离子的半径大小顺序为:W>Q>Z>Y
B.Z单质在氧气中燃烧后的产物不能使品红溶液褪色
C.单质熔点高低的顺序为:Z>Y>X
D.Z与W元素只能形成原子个数比为2:1的化合物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省清远市高二上学期10月月考化学试卷(解析版) 题型:填空题
已知下热化学方程式:
①H2(g)+1/2O2(g)= H2O(l) ⊿H= —285.8 kJ/mol
②H2(g)+1/2O2(g)= H2O(g) ⊿H= —241.8kJ/mol
③C(s)+1/2O2 (g) = CO (g) ⊿H= —110.5kJ/mol
④C(s)+ O2 (g) = CO2 (g) ⊿H= —393.5kJ/mol
回答下列问题:
(1)上述反应中属于放热的是
(2)H2的燃烧热为 ,C的燃烧热为
(3)燃烧10g H2生成液态水,放出的热量为
(4)CO的燃烧热为 ,其热化学方程式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com