
| A. | 增加反应物的量 | B. | 增大压强 | C. | 加热 | D. | 减小压强 |
科目:高中化学 来源: 题型:选择题
| A. | 钠在空气中燃烧,生成淡黄色的氧化钠粉末 | |
| B. | 钠是一种强还原剂,可以把钛从其盐溶液中置换出 | |
| C. | 将灼热的铜丝放入盛有氯气的集气瓶中,生成棕黄色的雾 | |
| D. | Fe(OH)3胶体具有吸附性,能吸附水中的悬浮颗粒并沉降,因而可用于净水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2溶液与少量Ca(OH)2溶液反应:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| B. | 向NaClO溶液中通入少量SO2:2ClO-+SO2+H2O═2HClO+SO32- | |
| C. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 用过量氨水吸收工业尾气中的SO2:2NH3•H2O+SO2═2NH4++SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表中金属元素与非金属元素交界线附近的元素既具有一定的金属性也具有一定的非金属性,所以它们属于过渡元素 | |
| B. | 若M2+和N2-的核外电子层结构相同,则原子序数:N>M | |
| C. | 元素周期表的短周期元素中,最外层电子数是其电子层数2倍的元素共有4种 | |
| D. | 在元素周期表中,原子序数差值为2的两种元素有可能处于同一主族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇的分子式:C2H5OH | B. | F-的结构示意图: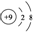 | ||
| C. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | D. | +4价的硫元素:S4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2的水溶液能导电,所以SO2是电解质 | |
| B. | 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 | |
| C. | 所有的共价化合物都是弱电解质,所有的离子化合物都是强电解质 | |
| D. | 强酸、强碱及大部分盐类都属于强电解质,弱酸、弱碱都属于弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
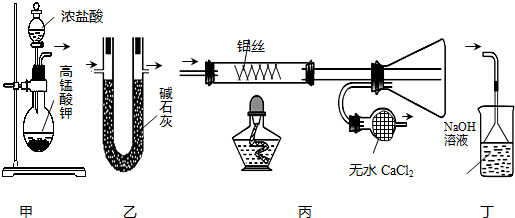
| A. | 用装置甲制取氯气 | B. | 用装置乙干燥氯气 | ||
| C. | 用装置丙制取并收集AlCl3 | D. | 用装置丁处理丙中排出的尾气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
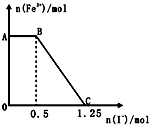 已知酸性高锰酸钾溶液可以将FeSO4氧化,化学反应的方程式为:2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的 物质的量的变化关系如图所示,则下列有关说法不正确的是( )
已知酸性高锰酸钾溶液可以将FeSO4氧化,化学反应的方程式为:2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的 物质的量的变化关系如图所示,则下列有关说法不正确的是( )| A. | 图中AB段主要是高锰酸钾和碘化钾溶液反应 | |
| B. | 图中BC段发生的反应为2Fe3++2I-═2Fe2++I2 | |
| C. | 根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25mol | |
| D. | 向C点以后的溶液中加入少量KSCN溶液,溶液变红色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com