
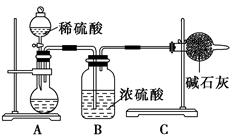
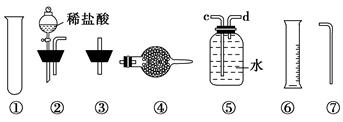
 =
=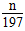 mol,则Na2CO3的质量分数为:
mol,则Na2CO3的质量分数为: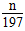 mol×106 g/mol÷m g=106n/197m。
mol×106 g/mol÷m g=106n/197m。

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.溶于水后加石灰水,看有无沉淀 |
| B.加热后称重,看质量是否变化 |
| C.加稀盐酸观察是否有气体产生 |
| D.在无色火焰上灼烧,观察火焰是否呈黄色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2Na2O2+2CO2→2Na2CO3+O2 | B.2Na2O2+2SO3→2Na2SO4+O2 |
| C.2Na2O2+H2SO4→Na2SO4+H2O2 | D.3Na2O2+Cr2O3→2Na2CrO4+Na2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.观察加热时是否放出气体 |
| B.观察滴加盐酸时能否放出气体 |
| C.溶于水中,再滴加石灰水,观察有无沉淀产生 |
| D.溶于水中,滴加少量的氯化钡溶液,观察有无白色沉淀产生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
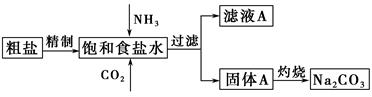
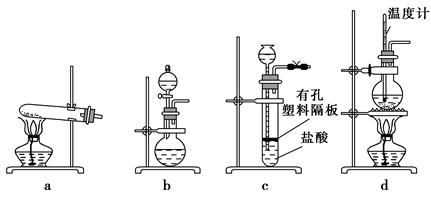
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.二氧化硫的排放会造成温室效应 |
| B.绿色食品是不含任何化学物质的食品 |
| C.Cu和浓H2SO4反应,H2SO4即表现氧化性,又表现酸性 |
| D.用加热的方法不能鉴别NaHCO3和Na2CO3固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.8 g ` | B.15.5 g |
| C.11.7 g | D.无法计算 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.NaOH与Na2CO3 | B.Na2CO3 |
| C.Na2CO3与NaHCO3 | D.NaHCO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.分别用砂锅加热两种样品,全部分解挥发没有残留物的是小苏打 |
| B.用洁净铁丝蘸取两种样品在煤气火焰上灼烧,使火焰颜色发生明显变化的是小苏打 |
| C.用两只小玻璃杯,分别加入少量的两种样品,再加入等量的食醋,产生气泡快的是小苏打 |
| D.先将两样品配成溶液,分别加入澄清石灰水,无白色沉淀生成的是小苏打 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com