
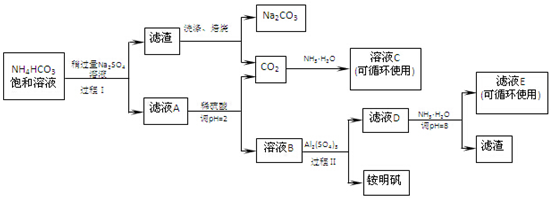
分析 碳酸氢铵溶液中加入硫酸钠,过滤得到滤渣与溶液A,而滤渣焙烧得到碳酸钠与二氧化碳,可知滤渣为NaHCO3,过程I利用溶解度不同发生复分解反应:2NH4HCO3+Na2SO4=2NaHCO3↓+(NH4)2SO4 ,滤液A中含有(NH4)2SO4 及溶解的NH4HCO3,加入硫酸,调节pH使NH4HCO3转化二氧化碳与(NH4)2SO4 ,得到溶液B为(NH4)2SO4 溶液,再加入硫酸铝得铵明矾,D中主要为剩余的NH4HSO4、Al2(SO4)3,用氨水调节pH得到氢氧化铝沉淀与硫酸铵,硫酸铵循环利用,二氧化碳用氨水稀释得到C溶液碳酸氢铵循环利用,据此分析解答.
解答 解:(1)溶液C中的溶质主要是NH4HCO3,故答案为:NH4HCO3;
(2)铵明矾溶液中铝离子水解:Al3++3H2O?Al(OH)3(胶体)+3H+,破坏水的电离平衡,溶液呈酸性,生成Al(OH)3(胶体)吸附水中杂质,可用于净水;
故答案为:酸; Al3++3H2O?Al(OH)3(胶体)+3H+;
(3)NH4HCO3易受热分解,故反应应控制温度不能超过40℃,
故答案为:NH4HCO3易受热分解;
(4)在平衡体系中增加一种反应物的浓度,反应正向进行,提高另外反应物的转化率,HCO32-(aq)+Na+(aq)?NaHCO3(s),Na+浓度增大平衡向正反应方向移,故答案为:HCO32-(aq)+Na+(aq)?NaHCO3(s),Na+浓度增大平衡向正反应方向移动;
(5)A为(NH4)2SO4和剩余的硫酸盐和碳酸盐,B主要为NH4HSO4,D主要为剩余的NH4HSO4、Al2(SO4)3,E为(NH4)2SO4,溶液E中的溶质离子为:NH4+、SO42-,故答案为:NH4+、SO42-;
(6)滤渣焙烧得到碳酸钠与二氧化碳,可知滤渣为NaHCO3,则焙烧的反应方程式为2NaHCO3$\frac{\underline{\;高温\;}}{\;}$ Na2CO3+CO2↑+H2O,故答案为:2NaHCO3$\frac{\underline{\;高温\;}}{\;}$ Na2CO3+CO2↑+H2O.
点评 本题考查制备实验方案设计、物质组成的测定,明确工艺流程原理是解题关键,综合考查学生分析解决问题的能力,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,7.8g Na2S和Na2O2的混合物中,阴离子所含电子数为1.8NA | |
| B. | 标准状况下,11.2LSO3中含有的分子数目为0.5 NA | |
| C. | 常温常压下,46gNO2与 N2O4的混合气体含有的氮原子数目无法计算 | |
| D. | 0.1 mo1•L-1 MgC12溶液中含有的Mg2+数目小于0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 反应物质 | 反应结果 | 影响因素 |
| A | Zn H2SO4 | H2 SO2 | 锌的还原性 |
| B | Na O2 | Na2O Na2O2 | 反应温度 |
| C | FeCl3溶液Na2S溶液 | 淡黄色或者黑色浑浊 | Na2S溶液加入量 |
| D | AlC13溶液 NaOH溶液 | 澄淸或者浑浊 | 试剂加入顺序 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在 16g18O2中含有NA个氧原子 | |
| B. | 16gCH4中含有4NA个C-H 键 | |
| C. | 22g 某气体含分子数为 0.5NA,则其摩尔质量为 44 | |
| D. | 含 NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为 1 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
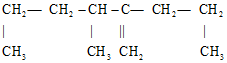 有机物,其正确命名应是( )
有机物,其正确命名应是( )| A. | 2,3-二丙基-1-丁烯 | B. | 2-丙基-3,5-二甲基-1-戊烯 | ||
| C. | 3-甲基-2-丙基-1-己烯 | D. | 3,5-二甲基-2-丙基-1-戊烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
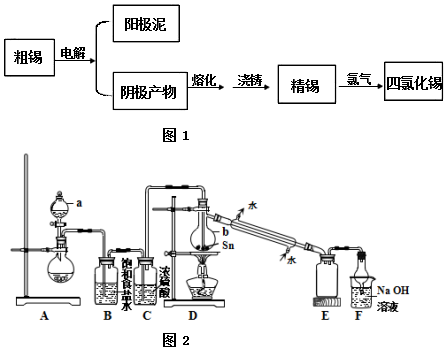
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com