
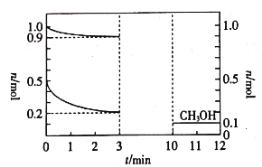
【题目】180℃时,将0.5 mol H2和1 mol CO2通入1L的恒容密闭容器中,反应生成甲醇蒸气(![]() )和某无机副产物,测得各物质的物质的量随时间的部分变化如图所示。下列说法中不正确的是( )
)和某无机副产物,测得各物质的物质的量随时间的部分变化如图所示。下列说法中不正确的是( )
A.该反应的化学方程式:![]()
B.在0~3 min内,![]() 的平均反应速率为
的平均反应速率为![]()
C.在3~10 min内,反应仍未达到平衡状态
D.10 min时,再通入0.5 mol H2和1 mol CO2,可提高H2和CO2的转化率
【答案】C
【解析】
A.由图可知,氢气和二氧化碳的物质的量的变化量为(0.5-0.2)mol=0.3mol和(1.0-0.9)mol=0.1mol,由质量守恒定律可知氢气和二氧化碳反应生成甲醇和水的反应为![]() ,故A正确;
,故A正确;
B.由图可知,二氧化碳的物质的量的变化量为(1.0-0.9)mol=0.1mol,由反应方程式可知,甲醇的物质的量的变化量为0.1mol,则甲醇的平均反应速率为![]() =
=![]() ,故B正确;
,故B正确;
C.由图可知,0~3 min时二氧化碳的物质的量的变化量为(1.0-0.9)mol=0.1mol,10 min时甲醇的物质的量为0.1mol,由反应方程式可知,甲醇的物质的量的变化量为0.1mol可知,3 min时反应达到平衡,则在3~10 min内,反应达到平衡状态,故C错误;
D.由反应方程式可知,该反应是一个气体体积减小的反应,若10 min时,再通入0.5 mol H2和1 mol CO2相当于增大压强,增大压强,平衡向正反应方向移动,氢气和二氧化碳的转化率增大,故D正确;
故选C。


科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期主族元素,它们在周期表中的相对位置如图所示,下列说法中正确的是( )
![]()
A.Y的价层电子排布式是![]()
B.四种元素所形成的最简单氢化物中,沸点最高的是可能Y的氢化物
C.Y、Z之间可形成离子型化合物
D.X、Z、W的最高价氧化物所对应的水化物不可能均是强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氮及其化合物的化工生产中,对有关反应的反应原理进行研究有着重要意义。
(1)t℃时,关于N2、NH3的两个反应的信息如下表所示:
化学反应 | 正反应活化能 | 逆反应活化能 | t℃时平衡常数 |
N2(g)+O2(g)=2NO(g) △H>0 | a kJ/mol | b kJ/mol | K1 |
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H<0 | c kJ/mol | d kJ/mol | K2 |
请写出t℃时氨气被一氧化氮氧化生成无毒气体的热化学方程式:______________________,t℃时该反应的平衡常数为__________ (用K1和K2表示)。
(2)工业合成氨的原理为:N2(g)+3H2(g)![]() 2NH3(g)下图甲表示在一定体积的密闭容器中反应时,H2的物质的量浓度随时间的变化。图乙表示在其他条件不变的情况下,起始投料H2与N2的物质的量之比(设为x)与平衡时NH3的物质的量分数的关系。
2NH3(g)下图甲表示在一定体积的密闭容器中反应时,H2的物质的量浓度随时间的变化。图乙表示在其他条件不变的情况下,起始投料H2与N2的物质的量之比(设为x)与平衡时NH3的物质的量分数的关系。

①图甲中0~t1 min内,v(N2)=_____mol·L-1·min-1;b点的v(H2)正_____a点的v(H2)逆(填“大于”“小于”或“等于”)。
②己知某温度下该反应达平衡时各物质均为1 mol,容器体积为1L,保持温度和压强不变,又充入3 mol N2后,平衡________(填“向右移动”“向左移动”或“不移动”)。
(3)①科学家研究出以尿素为动力的燃料电池新技术。用这种电池可直接去除城市废水中的尿素,既能产生净化的水,又能发电。尿素燃料电池结构如图所示,写出负极电极反应式:________________________________________________。
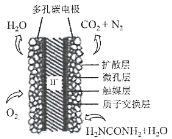
②理论上电池工作时,每消耗标准状况下2.24 L O2时,可产生的电量为________ (法拉第常数为96500C/ mol)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体胃酸的主要成分是盐酸。胃酸可助消化食物,但胃酸过多会损伤胃粘膜,使人感觉不适。抗酸药(又称抑酸剂)可以减少过多的胃酸。下列物质不属于抗酸药的是
A.胃得乐(主要成分:MgCO3)B.胃舒平[主要成分:Al(OH)3]
C.碳酸氢钠片(主要成分:NaHCO3)D.阿司匹林(主要成分: ![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某单烯烃A(C8H16)可以发生如下图示的转化,回答下列问题:

已知: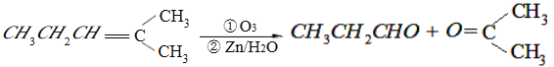
(1)B的分子式为___________________,D中含有官能团的名称___________________。
(2)B无银镜反应, D在浓硫酸存在下加热可得到能使溴水褪色且只有一种结构的物质E(不考虑立体异构),请写出E的结构简式____________________________________,D→E的反应类型___________________________。
(3)写出C→F的化学方程式_________________________________。
(4)H的同分异构体中,满足下列要求的结构一共有____________种(不考虑立体异构,包括H本身)
①属于酯类;②酸性条件下水解能得到相对分子质量为74的有机物
(5)已知: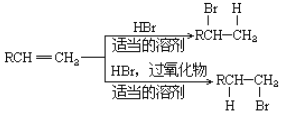 。
。
请写出由C制备2-丙醇的合成路线_____________________(无机原料任选)。合成路线流程图示例如下:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: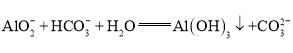 。向含0.01 mol
。向含0.01 mol ![]() 和0.02 mol NaOH的稀溶液中缓慢通入CO2,溶液中,
和0.02 mol NaOH的稀溶液中缓慢通入CO2,溶液中,![]() 随通入的
随通入的![]() 的变化如图,下列对应关系正确的是( )
的变化如图,下列对应关系正确的是( )
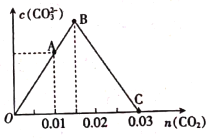
A.A点:![]()
B.B点:![]()
C.C点:![]()
D.O点:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳九芳烃是一种混合物,异丙苯就是其中的一种。工业上可用异丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如下。下列有关说法正确的是
![]()
A. a的同分异构体有7种B. a能发生取代反应、加成反应和氧化反应
C. b的分子式为![]() D. b、c互为同系物
D. b、c互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象、结论、因果关系均正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 向淀粉溶液中滴加稀硫酸,加热,再加碘水 | 溶液变蓝 | 淀粉没有水解 |
B | 将 |
| 有乙烯生成 |
C | 向 | 产生砖红色沉淀 | 葡萄糖具有还原性 |
D | 将乙醇加入浓硫酸中,快速加热到170℃,将产生的气体通入溴水 | 溴水褪色 | 不能证明有乙烯生成 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院科学家设计出一套利用SO2和太阳能综合制氢方案,其基本工作原理如图所示。下列说法错误的是
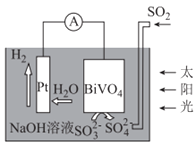
A.该电化学装置中,Pt电极作正极
B.Pt电极的电势高于BiVO4电极的电势
C.电子流向:Pt电极→导线→BiVO4电极→电解质溶液→Pt电极
D.BiVO4电极上的反应式为SO32--2e-+2OH-=SO42-+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com