
【题目】海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。
I.(1)海水中所得粗盐中通常含Ca2+、Mg2+、SO42-等杂质,为了得到精盐,下列试剂加入的先后顺序正确的是________
A.BaCl2→Na2CO3→NaOH→HCl B.NaOH→BaCl2→Na2CO3→HCl
C.BaCl2→NaOH→Na2CO3→HCl D. Na2CO3→NaOH→BaCl2→HCl
(2)为了检验精盐中是否含有SO42-,正确的方法是____________________________。
II.海藻中提取碘的流程如图所示
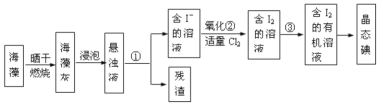
(1)灼烧过程中,需使用到的(除泥三角外)实验仪器有______
A.试管 B.瓷坩埚 C.坩埚钳 D.蒸发皿 E.酒精灯 F.三脚架
(2)指出提取碘的过程中有关实验操作名称:①________③__________④_________
(3)步骤②反应的离子方程式为___________________,该过程氧化剂也可以用H2O2,将等物质的量的I-转化为I2,所需Cl2和H2O2的物质的量之比为__________
(4)下列关于海藻提取碘的说法,正确的是_________
A.含碘的有机溶剂呈现紫红色
B.操作③中先放出下层液体,然后再从下口放出上层液体
C.操作④时,温度计的水银球应伸入液面以下但不能触碰到蒸馏烧瓶的底部
【答案】ABC 取少量精盐溶于水,先加入稀盐酸,无现象,向其中加入氯化钡溶液,若产生沉淀,则含有硫酸根离子 BCEF 过滤 萃取分液 蒸馏 Cl2+2I-=2Cl-+I2 1:1 A
【解析】
I.(1)Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,SO42-用氯化钡除去,最后过滤后向滤液加入盐酸酸化,但由于过量的氯化钡要用碳酸钠来除,所以碳酸钠必须放在氯化钡的后面,而氢氧化钠可以随意调整。
(2)为了检验精盐中是否含有SO42-,正确的方法是取少量精盐溶于水,先加入稀盐酸,无现象,向其中加入氯化钡溶液,若产生沉淀,则含有硫酸根离子。
II.(1)灼烧过程中,需使用到的(除泥三角外)实验仪器有瓷坩埚、坩埚钳、酒精灯、三脚架。
(2)①分离固体和液体用过滤,③将碘水中的碘单质萃取出来,萃取、分液即可,④从含碘的有机溶剂中获得晶态碘用蒸馏。
(3)步骤②反应的离子方程式为:Cl2+2I-=2Cl-+I2,如果用H2O2氧化I-,离子方程式为H2O2+2I-+2H+= I2+2H2O,由离子方程式可知将等物质的量的I-转化为I2,所需Cl2和H2O2的物质的量之比为1:1。
(4)A. 碘易溶在有机溶剂中,含碘的有机溶剂呈现紫红色。
B. 操作③中先放出下层液体,然后关闭活塞,再从上口放出上层液体。
C. 操作④时,温度计的水银球应放在蒸馏烧瓶的支管口处。
I.(1)Ca2+用碳酸钠除去,Mg2+用氢氧化钠除去,SO42-用氯化钡除去,最后过滤后向滤液加入盐酸酸化,但由于过量的氯化钡要用碳酸钠来除,所以碳酸钠必须放在氯化钡的后面,而氢氧化钠可以随意调整,故选ABC。
(2)为了检验精盐中是否含有SO42-,正确的方法是取少量精盐溶于水,先加入稀盐酸,无现象,向其中加入氯化钡溶液,若产生沉淀,则含有硫酸根离子,故答案为:取少量精盐溶于水,先加入稀盐酸,无现象,向其中加入氯化钡溶液,若产生沉淀,则含有硫酸根离子。
II.(1)灼烧过程中,需使用到的(除泥三角外)实验仪器有瓷坩埚、坩埚钳、酒精灯、三脚架,故答案为:BCEF。
(2)①分离固体和液体用过滤,③将碘水中的碘单质萃取出来,萃取、分液即可,④从含碘的有机溶剂中获得晶态碘用蒸馏,故答案为:过滤;萃取分液;蒸馏。
(3)步骤②反应的离子方程式为:Cl2+2I-=2Cl-+I2,如果用H2O2氧化I-,离子方程式为H2O2+2I-+2H+= I2+2H2O,由离子方程式可知将等物质的量的I-转化为I2,所需Cl2和H2O2的物质的量之比为1:1,故答案为:Cl2+2I-=2Cl-+I2;1:1。
(4)A. 碘易溶在有机溶剂中,含碘的有机溶剂呈现紫红色,故A正确;
B. 操作③中先放出下层液体,然后关闭活塞,再从上口放出上层液体,故B错误;
C. 操作④时,温度计的水银球应放在蒸馏烧瓶的支管口处,故C错误;
故选A。


科目:高中化学 来源: 题型:
【题目】(1)现有下列物质①NaCl晶体 ②液态SO2 ③纯醋酸④硫酸钡 ⑤铜 ⑥酒精(C2H5OH) ⑦熔化的KNO3 ⑧NaOH溶液 ⑨氨水 请用以上物质回答下列问题(填序号)。
在上述状态下能导电的强电解质是__________________; 属于弱电解质的是________________;属于非电解质,但溶于水后的水溶液能导电的是_________________。
(2)化学平衡移动原理同样也适用于其他平衡,已知在氨水中存在下列平衡:NH3·H2O ![]() NH4++OH-。
NH4++OH-。
①向氨水中加入NH4Cl固体时,平衡____________移动,(填“向右”或“向左”),c(OH-)____(填“增大”或“减小”,下同),c(NH4+)______。
②向氨水中加入MgCl2固体时,平衡_____移动,(填“向右”或“向左”),c(OH-)____(填“增大”或“减小”,下同),c(NH4+)_________。
③升高温度,c(OH-)______(填“增大”或“减小”,下同),c(NH4+)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“司乐平”是治疗高血压的一种临床药物,其有效成分M的结构简式如图所示。
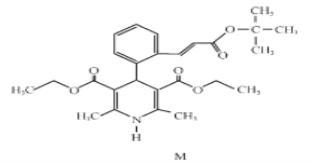
(1)下列关于M的说法正确的是______(填序号)。
a.属于芳香族化合物
b.遇FeCl3溶液显紫色
c.能使酸性高锰酸钾溶液褪色
d.1molM完全水解生成2mol醇
(2)肉桂酸是合成M的中间体,其一种合成路线如下:

已知: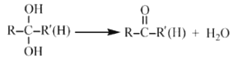
①烃A的名称为______。步骤I中B的产率往往偏低,其原因是__________。
②步骤III的反应类型是________。
③步骤Ⅳ反应的化学方程式为______________________________。
④肉桂酸的结构简式为__________________。
⑤C的同分异构体有多种,其中苯环上有一个甲基的酯类化合物有_____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由C、H、O组成的化合物8.80mg,完全燃烧后得二氧化碳22.0mg,水10.8mg。该化合物的实验式(最简式)是( )
A. C5H6OB. C5H12C. C5H12O2D. C5H12O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用40gNaOH固体溶于水配制成250ml溶液,此溶液的物质的量浓度是____,取该溶液10ml,再加水稀释成100ml时,所得稀溶液的物质的量浓度为___,在这100ml溶液中含____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是常见的硫氧化物,在化工、生活等领域中应用广泛。
I如图是实验室制取SO2并验证SO2某些性质的装置图
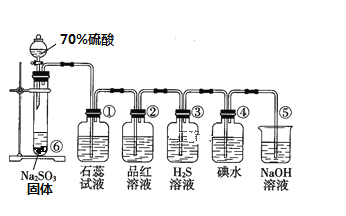
(1)⑥中发生反应的化学方程式为_________________________________
(2)③中实验现象为_____________________________________,证明SO2有____性
(3)⑤中离子反应方程式为______________________
II某学生对SO2与漂粉精的反应进行实验探究:
操作 | 现象 |
取4g漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
过滤,测漂粉精的pH | pH试纸先变蓝(约为12),后褪色 |
| i.液面上方出现白雾 ii.稍后,出现浑浊,溶液变为黄绿色 iii.稍后,产生大量白色沉淀,黄绿色褪去 |
(1)pH试纸颜色的变化说明漂粉精溶液具有的性质是_________________
(2)向水中持续通入SO2,未观察到白雾。推测现象i的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀。
①实验a的目的是_______________________________________________
②由实验a、b不能判断白雾中含有HCl,理由是_______________________________________
(3)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀盐酸,无明显变化。取上层清液,加入BaCl2溶液,产生白色沉淀,则沉淀X中含有的物质是___________
②用离子方程式解释现象iii中黄绿色褪去的原因 ___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
A. 2.0 mol·L-1 B. 1.5 mol·L-1 C. 0.18 mol·L-1 D. 0.24 mol·L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.焓变单位是kJmol1,是指1 mol物质参加反应时的能量变化
B.当反应放热时ΔH>0,反应吸热时ΔH<0
C.一个化学反应中,当反应物的总能量大于生成物的总能量时,反应放热,ΔH为“”
D.一个化学反应中,生成物总键能大于反应物的总键能时,反应吸热,ΔH为“+”
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com