
| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.015 mol/(L•s) | ||
| C. | v(C)=0.40 mol/(L•min) | D. | v(D)=0.45 mol/(L•min) |
分析 不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,注意单位要一致.
解答 解:不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,
A.$\frac{v(A)}{1}$=0.15mol/(L•min);
B.v(B)=0.015 mol/(L•s)=0.9 mol/(L•min),$\frac{v(B)}{3}$=0.3 mol/(L•min);
C.$\frac{v(C)}{2}$=0.20 mol/(L•min);
D.$\frac{v(D)}{2}$=0.225 mol/(L•min);
故反应速率v(B)>v(D)>v(C)>v(A),
故选B.
点评 本题考查化学反应速率快慢比较,难度不大,利用比值法可以迅速判断,也可以转化为同一物质表示的速率进行比较.


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:解答题
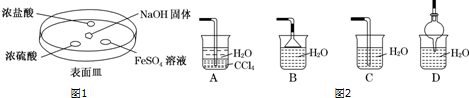
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
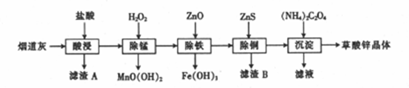
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 1.9 | 6.5 | 4.2 | 5.4 |
| 完全沉淀时的pH | 3.3 | 9.7 | 6.7 | 8.2 |
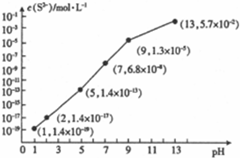
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向碘化钾溶液中加入用硫酸酸化的过氧化氢溶液:2I-+H2O2═I2+2OH- | |
| B. | 在亚硫酸中加入过量的次氯酸钠溶液:H2SO3+ClO-═Cl-+2H++SO42- | |
| C. | 向Ba(OH)2溶液中加入过量NH4HSO4:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+═2Fe3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L盐酸15mL | B. | 0.2mol/L盐酸12mL | ||
| C. | 0.15mol/L硫酸8mL | D. | 浓硫酸15mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原性:X的氢化物>Y的氢化物>Z的氢化物 | |
| B. | X、Y、M三种元素可形成离子化合物 | |
| C. | 简单离子的半径:M的离子>Z的离子>Y的离子>X的离子 | |
| D. | Z元素的最高价氧化物的水化物的化学式为HZO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打--Na2CO3 | B. | 消石灰--Ca (OH)2 | C. | 甲醛--CH3OH | D. | 大理石--CaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 硫酸的体积/mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
| 1 | 50.0 | 2.0 | 薄片 | 25 | 100 | m1 |
| 2 | 50.0 | 2.0 | 颗粒 | 25 | 70 | m2 |
| 3 | 50.0 | 2.0 | 颗粒 | 35 | 35 | m3 |
| 4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
| 5 | 50.0 | 2.0 | 粉末 | 35 | 30 | m5 |
| 6 | 50.0 | 2.0 | 粉末 | 25 | t6 | 16.1 |
| 7 | 50.0 | 2.0 | 粉末 | 25 | t7 | 16.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com