
【题目】电化学原理在工业生产、生活中有重要的作用
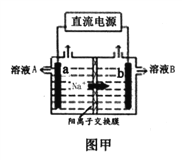
(1)图甲是工业上用惰性电极电解饱和食盐水的原理示意图,a电极为_______极,电极反应式为________,溶液B为_______溶液,电解总反应的离子方程式为_____________.标况下生成33.6Cl2,通过离子交换膜的Na+物质的量为__________.
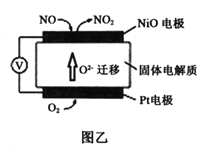
(2)通过NO传感器可检测NO的质量,其工作原理示意图如图乙。Pt电极上发生的是_________反应(填“氧化”或“还原”);写出NiO电极的电极反应式是______________。
【答案】 阳极 2Cl- -2e- = Cl2↑ NaOH 2Cl-+2H2O ![]() H2↑+Cl2↑+2OH- 3mol 还原 NO-2e-+ O2- =NO2
H2↑+Cl2↑+2OH- 3mol 还原 NO-2e-+ O2- =NO2
【解析】试题分析:本题考查氯碱工业的原理和计算,原电池原理的应用。
(1)电解池中,阳离子向阴极移动,图甲中Na+从左向右移动,则a电极为阳极,b电极为阴极。a电极上的电极反应式为:2Cl--2e-=Cl2↑。b电极上的电极反应式为2H++2e-=H2↑,阴极附近水的电离平衡被破坏,水的电离向电离方向移动,H+继续放电,b极附近c(OH-)![]() c(H+),溶液B为NaOH溶液。电解总反应的化学方程式为:2NaCl+2H2O
c(H+),溶液B为NaOH溶液。电解总反应的化学方程式为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,离子方程式为:2Cl-+2H2O
2NaOH+H2↑+Cl2↑,离子方程式为:2Cl-+2H2O ![]() H2↑+Cl2↑+2OH-。n(Cl2)=33.6L
H2↑+Cl2↑+2OH-。n(Cl2)=33.6L![]() 22.4L/mol=1.5mol,则通过离子交换膜的Na+的物质的量为3mol。
22.4L/mol=1.5mol,则通过离子交换膜的Na+的物质的量为3mol。
(2)原电池中阴离子向负极移动,根据图乙中O2-的迁移方向判断,Pt电极为正极,NiO电极为负极。由于Pt电极为正极,Pt电极上发生得电子的还原反应,电极反应式为:O2+4e-=2O2-。NiO电极上NO失电子被氧化成NO2,电极反应式为:NO-2e-+O2-=NO2。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】在某密闭容器中,发生如下反应:2NO(g)+O2(g) ![]() 2NO2(g) △H<0 。下列研究目的和示意图相符的是( )
2NO2(g) △H<0 。下列研究目的和示意图相符的是( )
A | B | C | D | |
目的 | 压强对反应的影响(P1>P2) | 温度对反应的影响 | 平衡体系增加O2对反应的影响 | 催化剂对反应的影响 |
图示 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中。下列分析正确的是( )

A. K1闭合,铁棒上发生的反应为2H++2e-→H2↑
B. K1闭合,石墨棒周围溶液pH逐渐升高
C. K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D. K2闭合,电路中通过0.002NA个电子时,两极共产生0.001mol气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是一种新型清洁能源。回答问题:
(1)101KPa、25℃时,燃烧32g液态甲醇生成液态水和二氧化碳放热726.5kJ,则甲醇燃烧的热化学方程式为_____________
已知:2CH3OH(g)=CH3OCH3(g)+H2O(g) △H=-24.5kJ·mol-1
CO(g)+2H2(g)![]() CH3OH(g) △H=akJ·mol-1
CH3OH(g) △H=akJ·mol-1
则2CO(g)+4H2(g)= CH3OCH3(g)+H2O(g) △H=__________
(2)工业上可用CO和H2制取甲醇,其热化学反应方程式为:CO(g)+2H2(g)![]() CH3OH(g) △H=akJ·mol-1,CO在不同温度下的平衡转化率与压强的关系如下图所示
CH3OH(g) △H=akJ·mol-1,CO在不同温度下的平衡转化率与压强的关系如下图所示
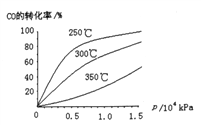
①△H______0(填“﹥”或“<”).判断依据是___________________
②为提高CO转化率,可采取的措施是_____________________________(至少答出两条)
③实际生产中,反应的条件控制在250℃,1.3×104kPa左右,选择此压强的理由是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 反应NH3(g)+HCl(g)![]() NH4Cl(s)能自发进行,则该反应△H>0
NH4Cl(s)能自发进行,则该反应△H>0
B. 氨水溶液加水稀释后,溶液中 的值减小
的值减小
C. 1L1 molL-1的NaClO溶液中含有ClO-的数目为6.02×1023
D. 一定条件下,反应2SO2(g)+O2(g)![]() 2SO3(g)△H<0达到平衡后,升高体系温度,反应重新达到平衡前,有2v正(O2)>v逆(SO3)
2SO3(g)△H<0达到平衡后,升高体系温度,反应重新达到平衡前,有2v正(O2)>v逆(SO3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com