
| A. | 1mol FeCl3完全转化为Fe(OH)3胶体后生成NA个胶体粒子 | |
| B. | 在MnO2的作用下,1mol H2O2充分反应转移2NA个电子 | |
| C. | 在标准状况下,22.4L H2和4g He均含有NA个分子 | |
| D. | 46g NO2与92g N2O4均含有3NA个原子 |
分析 A、一个氢氧化铁胶粒是多个氢氧化铁的聚集体;
B、双氧水的分解为歧化反应;
C、氦气为单原子分子;
D、分别求出二氧化氮和四氧化二氮的物质的量,然后根据二氧化氮为三原子分子,而四氧化二氮为6原子分子来分析.
解答 解:A、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故1mol氯化铁所形成的胶粒的个数小于NA个,故A错误;
B、双氧水的分解为歧化反应,故1mol双氧水分解转移1mol电子即NA个,故B错误;
C、氦气为单原子分子,故4g氦气的物质的量为1mol,含NA个氦气分子;而标况下22.4L氢气的物质的量为1mol,也含NA个分子,故C正确;
D、46g二氧化氮的物质的量为1mol,而二氧化氮为三原子分子,故1mol二氧化氮中含3mol原子,92g二氧化氮的物质的量为1mol,而四氧化二氮为6原子分子,故1mol四氧化二氮含6mol原子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 容器内压强不变 | |
| B. | 单位时间内消耗1molH2,同时生成2molHI | |
| C. | 混合气体的颜色不变 | |
| D. | HI的浓度与I2的浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,试写出:
,试写出:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 颜色、性质 | 物质 | 颜色、性质 |
| 氢氧化铜Cu(OH)2 | 蓝色固体不溶于水 | 硫酸铜(CuSO4) | 溶液呈蓝色 |
| 氧化亚铜(Cu2O) | 红色固体不溶于水 | 氯化铜(CuCl2) | 浓溶液呈绿色,稀溶液呈蓝色 |
| 氯化亚铜(CuCl) | 白色固体不溶于水 | 碱式氯化铜 | 绿色固体不溶于水 |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
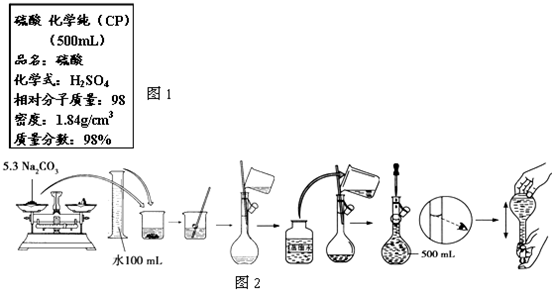
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1}{n}$mol-1 | B. | 8n mol-1 | C. | 4n mol-1 | D. | n mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在家用燃煤中加入适量的生石灰能有效减少二氧化硫的排放 | |
| B. | 石英、玛瑙、太阳能电池的主要成分均为二氧化硅 | |
| C. | 海水中含有丰富的资源,不经化学反应可从海水中提取溴、镁、氯化钠等物质 | |
| D. | 直馏汽油、裂化汽油、植物油、甘油均能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com