
| 一定条件下 |
 ,发生的是加聚反应,
,发生的是加聚反应,| 一定条件下 |
 ;加聚反应;
;加聚反应;
| ||
| ||
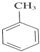 +3HNO3
+3HNO3| 浓硫酸 |
| △ |
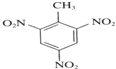 +3H2O,该反应为取代反应,
+3H2O,该反应为取代反应, +3HNO3
+3HNO3| 浓硫酸 |
| △ |
 +3H2O;取代反应.
+3H2O;取代反应.


科目:高中化学 来源: 题型:
 已知实验室制取氯气是用二氧化锰和浓盐酸反应的原理,在收集时,若是用排水法,可能会损失部分氯气.
已知实验室制取氯气是用二氧化锰和浓盐酸反应的原理,在收集时,若是用排水法,可能会损失部分氯气.| 仪器标号 | C | D | E | F | G |
| 仪器 | 洗气瓶 | 洗气瓶 | 硬质玻璃管,加热 | 干燥管 | 干燥管 |
| 仪器中所加物质 | NaOH溶液 | 浓硫酸 | CuO粉末 | 试剂X | 无水CaCl2固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |
 |
 |
 |
 |
 |
| 序号 | a | b | c | d | e | f |

| 温度 实验次数 |
超始温度t1/℃ | 终止温度t2/℃ | 平均温度差 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学兴趣小组要完成中和热的测定.
某化学兴趣小组要完成中和热的测定.| 实 验 用 品 | 溶 液 温 度 | 中和热△H(平均值) | ||
| t1 | t2 | |||
| ① | 50mL0.55mol?L-1NaOH 50mL.0.5mol?L-1HCl |
20℃ | 23.3℃ | |
| ② | 50mL0.55mol?L-1NaOH 50mL.0.5mol?L-1HCl |
20℃ | 23.5℃ | |
查看答案和解析>>
科目:高中化学 来源: 题型:
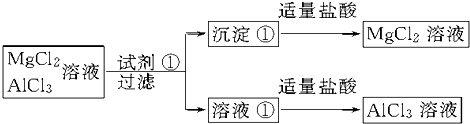
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 被提纯物质 | 除杂试剂 | 分离方法 | |
| A | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| B | CO2(SO2) | 饱和Na2CO3溶液 | 洗气 |
| C | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| D | 溴苯(溴) | 氢氧化钠溶液 | 分液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com