
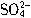 所带电荷数是Na+所带电荷数的3/5倍
所带电荷数是Na+所带电荷数的3/5倍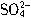 与Cl-的物质的量之和等于Na+的物质的量
与Cl-的物质的量之和等于Na+的物质的量科目:高中化学 来源: 题型:阅读理解
| +4 |
| S |
| +6 |
| S |

| 3.16nv |
| m |
| 3.16nv |
| m |
查看答案和解析>>
科目:高中化学 来源: 题型:
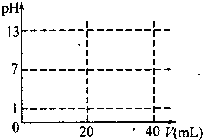 (2012?成都模拟)溶液中的化学反应大多是离子反应.根据要求回答下列问题.
(2012?成都模拟)溶液中的化学反应大多是离子反应.根据要求回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | N≡N | H-H | N-H |
| 键能kJ?mol-1 | 946 | 436 | 390 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com