
分析 化合价升高元素所在的反应物是还原剂,实现化合价的升高要加入氧化剂,化合价降低元素所在的反应物是氧化剂,实现化合价的降低要加入还原剂.
解答 解:(1)FeCl2→FeCl3,铁元素化合价升高了,所以需加入氧化剂才能实现,比如FeCl2与氯气反应,故答案为:氧化;氯气;
(2)CuO→Cu,铜元素的化合价降低了,所以需要加入还原剂才能实现,如氢气、一氧化碳等,故答案为:还原;CO(H2);
(3)HCl→Cl2是氯元素的化合价升高了,所以需加入氧化剂才能实现,发生氧化反应,HCl是还原剂,故答案为:氧化;还原;
(4)H2SO4→H2,氢元素的化合价降低了,所以H2SO4是氧化剂,发生了还原反应,故答案为:还原;氧化.
点评 本题考查学生氧化还原反应中的有关概念知识,可以根据所学知识来回答,较简单.


科目:高中化学 来源: 题型:推断题
 .
. ,元素D在元素周期表中的位置是第三周期VIIA族.
,元素D在元素周期表中的位置是第三周期VIIA族.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
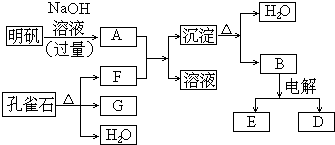
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | 0 | 10 | 20 | 30 | 40 |
| c(H2O2) mol•L-1 | 0.80 | 0.40 | 0.20 | 0.10 | 0.05 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度的硅晶体广泛用于制造光导纤维材料 | |
| B. | 燃烧化石燃料产生的废气中含有 SO2,会造成大气污染,使雨水 pH=5.6形成酸雨 | |
| C. | “春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是蛋白质和烃 | |
| D. | 海轮外壳上镶入铜块,可以延缓船体腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
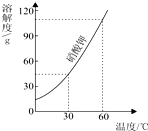
| A. | 硝酸钾的溶解度随温度的升高而增大 | |
| B. | 降低温度可以使接近饱和的硝酸钾溶液变饱和 | |
| C. | 60℃时120g硝酸钾与100g水充分混合可以形成饱和溶液 | |
| D. | 60℃时硝酸钾溶液中溶质质量分数一定大于30℃时硝酸钾溶液中溶质质量分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①②④ | D. | ②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com