
| A. | CH3COONa与CH3COOH混合溶液呈中性,则溶液中有c(CH3COO-)═c (Na+) | |
| B. | NaHCO3溶液中有:c (H+)+c (H2CO3)═c (OH-)+c (CO32-) | |
| C. | 物质的量浓度均为0.1 mol/L的Na2CO3和NaHCO3的混合溶液中有:c (Na+)>c (HCO3-)>c (CO32-)>c (OH-)>c (H+) | |
| D. | 常温下,p H为2的某酸HA与pH为12的某碱BOH等体积混合溶液呈酸性,则HA为强酸BOH为弱碱 |
分析 A.CH3COONa与CH3COOH混合溶液呈中性,c(H+)=c(OH-),结合溶液中电荷守恒分析判断;
B.NaHCO3溶液中存在物料守恒和电荷守恒,据此计算判断;
C.物质的量浓度均为0.1 mol/L的Na2CO3和NaHCO3的混合溶液中,碳酸钠水解程度大于大于碳酸氢钠;
D.常温下,p H为2的某酸HA与pH为12的某碱BOH等体积混合溶液呈酸性,说明HA溶液中存在电离平衡;
解答 解:A.CH3COONa与CH3COOH混合溶液呈中性,c(H+)=c(OH-),溶液中电荷守恒为c(H+)+c(Na+)=c(OH-)+c(CH3COO-),溶液中有c(CH3COO-)═c (Na+),故A正确;
B.NaHCO3溶液中存在物料守恒c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3),电荷守恒c(H+)+c(Na+)=c(HCO3-)+c(CO32-)+c(OH-),据此计算得到c (H+)+c (H2CO3)═c (OH-)+c (CO32-),故B正确;
C.物质的量浓度均为0.1 mol/L的Na2CO3和NaHCO3的混合溶液中,碳酸钠水解程度大于大于碳酸氢钠溶液显碱性,离子浓度大小c (Na+)>c (HCO3-)>c (CO32-)>c (OH-)>c (H+),故C正确;
D.常温下,p H为2的某酸HA与pH为12的某碱BOH等体积混合溶液呈酸性,说明HA溶液中存在电离平衡,证明酸一定为弱酸,故D错误;
故选D.
点评 本题考查了电解质溶液中电荷守恒、物料守恒、盐类水解和弱电解质电离平衡的分析判断,掌握基础是解题关键,题目难度中等.


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:选择题
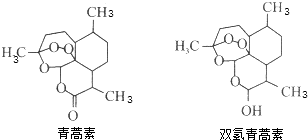
| A. | 青蒿素的分子式为C15H20O5 | |
| B. | 1 mol青蒿素最多能和1 molBr2发生加成反应 | |
| C. | 双氢青蒿素能发生氧化反应、酯化反应 | |
| D. | 青蒿素转化为双氢青蒿素发生了氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ○ |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚氯乙烯的单体是CH3CH2Cl | |
| B. | 聚氯乙烯是高分子化合物 | |
| C. | 聚氯乙烯能够使溴的四氯化碳溶液褪色 | |
| D. | 聚氯乙烯保鲜膜最适合用来包装蔬菜、水果及熟食 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com