
��������̼����Ԫ����ɵĺϽ�ijʵ��С��Ϊ���о��úϽ�����ʲ��ⶨ�úϽ���̼���������������������ʵ�鷽����ʵ��װ�ã�

��.̽���úϽ��ijЩ���ʣ�
(1)ȡa g�Ͻ��ĩ����������ƿ������������Ũ���ᣬA��B�о�����������ԭ����_________________________________________________________________��
(2)��ȼ�ƾ���һ��ʱ���A�о��ҷ�Ӧ����д��A�з�Ӧ�Ļ�ѧ����ʽ��____________________________________________________________________________
________________________________________________________________________��
(3) ��ʢ��BaCl2��Һ��C�Թ��У����˵��ܿ��������⣬��������������������ֳ����ݣ��ֱ�μ�������Һ�������������Ļ�ѧʽ�����±���Ӧ��λ�á�
| �μӵ���Һ | ��ˮ | ��ˮ |
| �����Ļ�ѧʽ |
��.�ⶨ��Ʒ��̼������������
(4)װ��F��������_______________________________________________________��
(5)��Ӧ��������U�ι�E����m g����Ͻ���̼����������Ϊ________(�ú�m��a��ʽ�ӱ�ʾ)����û��װ��D����ʹ�Ͻ���̼����������______ (��ƫ�ߡ�ƫ�͡���Ӱ��)
(6)����SO2����ͨ�뺬��n mol Na2S����Һ�У���Һ�г��ֻ�ɫ���ǣ��Է�������Һ���������SO2����________mol(�������ܽ��SO2)��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ú�����г����о���ͬ�¶���ƽ�ⳣ����Ͷ�ϱȼ���ֵ�����⣮
��֪��CO��g��+H2O��g�� H2��g��+CO2��g��ƽ�ⳣ�����¶ȵı仯���±���
H2��g��+CO2��g��ƽ�ⳣ�����¶ȵı仯���±���
| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
�Իش��������⣺
��800�淢��������Ӧ���Ա��е����ʵ���Ͷ����ݷ�Ӧ��������������Ӧ�����ƶ����С�����ѡ��A��B��C��D��E����
| n��CO�� | n��H2O�� | n��H2�� | n��CO2�� | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 2 | 1 | 2 | 3 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
��1L�ܱ�������ͨ��10 molCO��10 molˮ����,��500���¾���30s��
��ƽ��,��30s��CO��ƽ����Ӧ����Ϊ��
��3����֪��һ���¶��£�C��s��+CO2��g�� 2CO��g��ƽ�ⳣ��K��K�ı���ʽ������
2CO��g��ƽ�ⳣ��K��K�ı���ʽ������
C��s��+H2O��g�� CO��g��+ H2��g��ƽ�ⳣ��K1��
CO��g��+ H2��g��ƽ�ⳣ��K1��
CO��g��+H2O��g�� H2��g��+ CO2��g��ƽ�ⳣ��K2��
H2��g��+ CO2��g��ƽ�ⳣ��K2��
��K��K1��K2֮��Ĺ�ϵ�ǣ��� ��
ij�¶ȡ��ݻ��̶������У�Ͷ��һ����Ӧ��Կ��淴Ӧ
C��s��+ CO2��g�� 2CO��g�������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬���ǡ�
2CO��g�������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬���ǡ�
A��c��CO2��= c��CO�� B�����������Է�����������
C.�����е�ѹǿ���� D.v����CO��= 2v����CO2�� E.c��CO�����ֲ���
��5����ͼ1��ʾ���ڼס����������ж�����1mol C��1mol CO2����ʹ�ס���
��������ʼ�ݻ����.����ͬ�¶��·�����ӦC(s)+CO2(g)  2CO(g)��
2CO(g)��
��ά�ַ�Ӧ�������¶Ȳ��䣮��֪��������CO2��ת������ʱ��仯��
ͼ����ͼ2��ʾ,����ͼ2�л�����������CO2��ת������ʱ��仯��ͼ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й���ҩ���ʹ��˵����ȷ����
A����˾ƥ����һ���θ�ðҩ�����н�����ʹ����
 B��ʹ����ù��ʱ�����ý���Ƥ�Կ�ֱ�Ӿ���ע��
B��ʹ����ù��ʱ�����ý���Ƥ�Կ�ֱ�Ӿ���ע��
C�����ð�˾ƥ�ֳ���θ������Ӧ���ж����֣�Ӧ����ͣҩ������ע��NaHCO3��Һ
D��θ�����IJ��˶����Է����������ơ�����������̼���Ƶ��к�θ���ҩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪X��Y��Z��W��Ϊ��ѧ��ѧ�г����ĵ��ʻ������֮���ת����ϵ��ͼ��ʾ(���ֲ�������ȥ)����W��X��������:

| ѡ�� | A | B | C | D |
| X | C | Fe | Ca(OH)2��Һ | AlCl3 |
| W | O2 | HNO3 | CO2 | NH3��H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ������480 mL 1.0 mol/L��NaOH��Һ������������������ȷ����ģ��������������������Һ��Ũ��ƫ�ߵ���:
A����ȡ��������20.0 g B������ʱ���ӹ۲�̶���
C����Һʱ���������ܽ��������Ƶ��ձ�û�н��г�ϴ
D����Һ�ò���������ʱ���������¶˿�������ƿ�̶����Ϸ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ���������ϴ������¹�ϵ��
 | |||||
 | |||||
 | |||||
������ϵ ���й�ϵ �����ϵ
�����и����˵����ȷ����
A���������ǵ�������ڰ�����ϵ B����������������������ڰ�����ϵ
C�������뻯�������ڽ����ϵ D��������ԭ��Ӧ��ֽⷴӦ���ڲ��й�ϵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и��������У�����������ԭ��Ӧ�����������������
A��Fe3����H����SO ��ClO�� B��Fe3����Fe2����SO
��ClO�� B��Fe3����Fe2����SO ��OH��
��OH��
C��Al3����Na����SO ��HCO3�� D��K����H����I����MnO
��HCO3�� D��K����H����I����MnO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£���H2O2��Һ�еμ�����FeSO4��Һ���ɷ�������������Ӧ��
2Fe2++H2O2+2H+��2Fe3++2H2O 2Fe3++H2O2��2Fe2++O2��+2H+ ���ɴ�˵����
(1)H2O2�������Ա�Fe3+���������仹ԭ�Ա�Fe2+���������ǿ����������
(2)��H2O2�ֽ�����У�FeSO4��Һ ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȡ�����࣬���������������̣�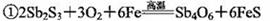
�� ���ڷ�Ӧ�١��ڵ�˵������ȷ����
���ڷ�Ӧ�١��ڵ�˵������ȷ����
A.��Ӧ����SbԪ�ر�����
B����Ӧ����SbԪ�ر���ԭ
C.��״���£�ÿ����4 mol Sbʱ������67.2LO2
D.��Ӧ��˵��������C�Ļ�ԭ�Ա�Sbǿ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com