

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题
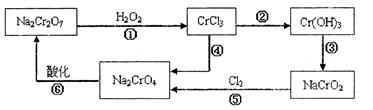
 已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38。试回答:
已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38。试回答:
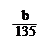 mol
mol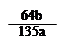 ×100℅
×100℅ 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2 NH3 (g); △H <0, 该反应应采取的适宜条件是( )
2 NH3 (g); △H <0, 该反应应采取的适宜条件是( )| A.低温、高压、催化剂 | B.适宜的温度、高压、催化剂 |
| C.低温、常压、催化剂 | D.适宜的温度和压强、催化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
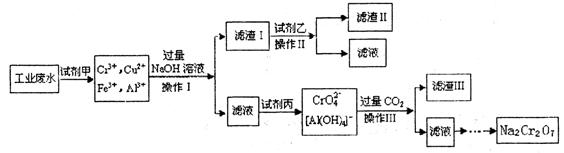
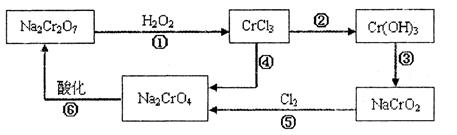
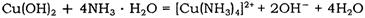
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
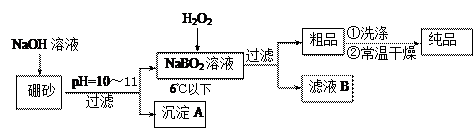
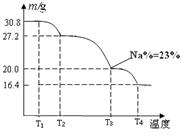
 体中将混有NaBO2 ,则产品中钠的质量分数 ▲ (填 “升高”、“降低”或“不变”)。
体中将混有NaBO2 ,则产品中钠的质量分数 ▲ (填 “升高”、“降低”或“不变”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.石英玻璃的结构类似于液体 |
| B.石英玻璃和石英都属于原子晶体 |
| C.石英玻璃和石英耐高温且能抵抗一切酸的腐蚀 |
| D.石英玻璃能经受高温剧变且能抗碱的腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
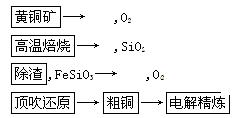
 到了NO和NO2的混合气体8.736L,与3.304LO2混合后,得到的混合气体恰好被水完全吸收。
到了NO和NO2的混合气体8.736L,与3.304LO2混合后,得到的混合气体恰好被水完全吸收。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
A.氯碱工业中阳离子交换膜的主要作用是:防止阳极产生的氯气和阴极产生的 氢气及氢氧化钠反应 氢气及氢氧化钠反应 |
| B.硫酸工业中合成SO3通常采用常压,是因为常压比高压更有利于SO3的生成 |
| C.电解精炼铜时,纯铜作为阳极,粗铜作为阴极 |
| D.工业合成氨通常采用500℃的高温主要是为了提高氮气的转化率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 后产物可以用于漂白消毒。根据以上信息完成下列化学方程式:
后产物可以用于漂白消毒。根据以上信息完成下列化学方程式:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com