
【题目】下列有关热化学方程式的叙述中,不正确的是
A.含20.0g NaOH的稀溶液与稀盐酸完全中和放出28.7 kJ的热量,则表示该反应中和热的热化学方程式为NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1) H=-57.4kJmol-1
B.根据C(石量,s)=C(金刚石,s) H>0 可知石墨比金刚石稳定
C.根据2H2(g)+O2(g)=2H2O(l) H=-483.6 kJmol-l可知H2的燃烧热为241.8kJmol-1
D.由C(s)+O2(g)=CO2(g) H1,C(s)+![]() O2(g)=CO(g) H2 可知 H1>H2
O2(g)=CO(g) H2 可知 H1>H2
【答案】D
【解析】
A.依据酸碱中和热概念是强酸强碱在稀溶液反应生成1mol水放出的热量计算分析,20.0g NaOH的物质的量是0.5mol,含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则1molNaOH即40gNaOH完全反应放热57.4 kJ,所以表示中和热的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1) H=-57.4kJmol-1,A正确;
B.根据C(石墨,s)=C(金刚石,s)△H>0,可知石墨的能量低于金刚石的能量,物质具有的能量越低越稳定,所以石墨比金刚石稳定,B正确;
C.氢气的燃烧热是lmol氢气完全燃烧生成稳定氧化物液态水放出的热量,由题目已知的热化学方程式可知H2的燃烧热为241.8kJmol-1,C正确;
D.物质C燃烧反应是放热反应,完全燃烧放出的能量比不完全燃烧放出的能量多,但是反应是放热的,焓变是带有负号的,反应放出的热量越多,反应热就越小,所以△H1<△H2,D错误;
故合理选项是D。


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】在100℃时,将0.40 mol二氧化氮气体充入一个2 L抽空的密闭容器中,发生反应:2NO2 N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)在上述条件下,从反应开始至20 s时,用NO2表示的平均反应速率为__________mol·L1·s1。
(2)n3________(填“>”“<”或“=”)n4;该反应的平衡常数K的数值为___________(精确到0.1)。
(3)若在相同条件下最初向该容器中充入N2O4,要达到上述平衡状态,N2O4的起始浓度是______mol·L1。
(4)上述(3)达到平衡后N2O4的转化率为______________,混合气体的平均摩尔质量为______________。
(5)达到平衡后,如果升高温度,气体颜色会变深,则升高温度后,反应2NO2N2O4的平衡常数将_______________(填“增大”“减小”或“不变”)。
(6)达到平衡后,如果向该密闭容器中再充入0.32 mol He,并把容器体积扩大为4 L,则平衡将______________(填“向左移动”“向右移动”或“不移动”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,有体积相同的四种溶液:①pH=3的CH3COOH溶液 ②pH=3的盐酸 ③pH=11的氨水 ④pH=11的NaOH溶液。下列说法不正确的是( )
A. 若将四种溶液稀释100倍,稀释后溶液pH大小顺序:③>④>②>①
B. 等体积的②和③混合生成强酸弱碱盐,混合后溶液呈酸性
C. 等体积的③和④分别用等浓度的硫酸溶液中和,消耗硫酸溶液的体积:③>④
D. 等体积的①和②分别与足量的锌粒反应生成的氢气在同温同压下体积:①>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图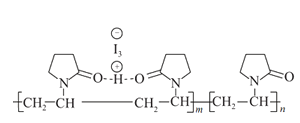 ,下列说法不正确的是( )
,下列说法不正确的是( )
A.聚维酮的单体是![]() B.聚维酮分子由(m+n)个单体聚合而成
B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质D.聚维酮在一定条件下能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在-定体积的某密闭容器中发生合成氨反应:N2(g)+3H2(g) ![]() 2NH3(g) △H<0。673K,30MPa下,n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述不正确的是( )
2NH3(g) △H<0。673K,30MPa下,n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述不正确的是( )
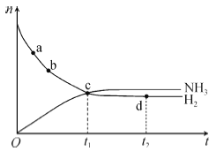
A.a点的正反应速率大于b点的
B.c点处,υ正(N2)=υ逆(N2)
C.d点处,υ正(N2):υ逆(H2)=1:3
D.升高温度,反应至t2时刻,n(H2)比图中d点的值大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙基丹皮酚肟胺基醇醚衍生物(H)具有很好的抗血小板聚集活性,是良好的心脑血管疾病的治疗药物。
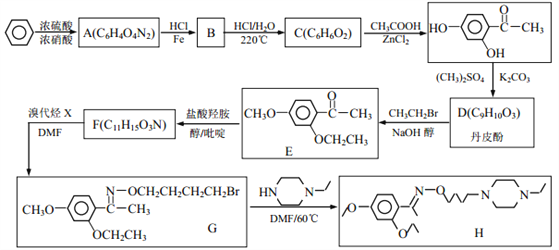
已知:①![]()
②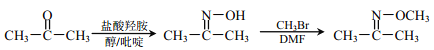
③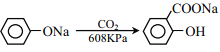
请回答:
(1)E中含有的官能团名称为_________;
(2)丹皮酚的结构简式为_________;
(3)下列说法不正确的是(___)
A.乙基丹皮酚肟胺基醇醚衍生物 H 的分子式为 C21H34O3N3
B.物质B 可能溶于水,且能与盐酸反应生成有机盐
C. D→E 和 G→H 的反应类型均为取代反应
D.物质 C 能使浓溴水褪色,而且 1mol C 消耗 2molBr2
(4)写出 F→G 的化学方程式_________。
(5)写出满足下列条件 F 的所有同分异构体的结构简式_________。
①能发生银镜反应;1molF 与 2molNaOH恰好反应。
②1H-NMR 谱显示分子中含有 5 种氢原子; IR 谱显示有-NH2,且与苯环直接相连。
(6)阿司匹林也具有抑止血小板凝聚的作用。结合题给信息,请以硝基苯和乙酸酐为原料设计合理的路线制备阿司匹林(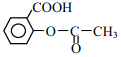 )。(用流程图表示,无机试剂任选)______。
)。(用流程图表示,无机试剂任选)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的四种短周期主族元素,A、B、C、D、E为上述四种元素中的两种或三种所组成的化合物。已知A的相对分子质量为28,B分子中含有18个电子,五种化合物间的转化关系如图所示。下列说法错误的是( )
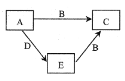
A. X、Y组成化合物的沸点一定比X、Z组成化合物的沸点低
B. Y的最高价氧化物的水化物为弱酸
C. Y、Z组成的分子可能为非极性分子
D. W是所在周期中原子半径最小的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求完成下列各小题:
Ⅰ.(1)理论上稀的强酸、强碱反应生成1mol H2O(l)时放出57.3kJ的热量,写出表示稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式________ 。
(2)已知:乙苯催化脱氢制苯乙烯反应:苯在计算键能时,此处可看作为![]() ,
, ![]()
![]()
![]() +H2(g)
+H2(g)
化学键 | C—H | C—C | C=C | H—H |
键能/kJ·mol-1 | 412 | 348 | 612 | 436 |
计算上述反应的ΔH=________ kJ·mol-1。
Ⅱ.25 ℃时,部分物质的电离平衡常数如表所示,请回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为_______。
(2)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池如图所示,a、b均为惰性电极。下列叙述不正确的是
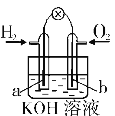
A.a极是负极,该电极上发生氧化反应
B.b极反应是O![]() +4OH
+4OH![]() -4e
-4e![]() =2H
=2H![]() O
O
C.总反应方程式为2H![]() +O
+O![]() =2H
=2H![]() O
O
D.氢氧燃料电池是一种具有应用前景的绿色电源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com