
·ÖĪö £Ø1£©4.9gĮņĖįµÄĪļÖŹµÄĮæŹĒ0.05mol£¬ĆæøöĮņĖį·Ö×ÓÖŠŗ¬ÓŠ2øöHŌ×Ó”¢4øöOŌ×Ó£¬øł¾ŻN=nNA¼ĘĖćŗ¬ÓŠOŌ×ÓŹż£»ĆæøöĖ®·Ö×ÓÖŠŗ¬ÓŠ1øöOŌ×Ó£¬ŌņĮņĖįŗĶĖ®ÖŠOŌ×ÓøöŹżĻąµČŹ±ĮņĖįŗĶĖ®µÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ4£¬øł¾Żm=nM¼ĘĖćĖ®µÄÖŹĮ棻
£Ø2£©±źæöĻĀ£¬44.8L¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæ=$\frac{44.8L}{22.4L/mol}$£¬øł¾Żm=nM¼ĘĖ涞Ńõ»ÆĢ¼ÖŹĮ棻Ćæøö·Ö×ÓÖŠŗ¬ÓŠµÄÖŹ×ÓŹżŹĒ22£¬øł¾ŻN=nNA¼ĘĖćŗ¬ÓŠµÄÖŹ×ÓŹż£»
£Ø3£©Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬ĘųĢåĦ¶ūĢå»żĻąµČ£¬ĻąĶ¬Ģå»żµÄCOŗĶ¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæĻąµČ£¬øł¾ŻN=nNA¼ĘĖćĘä·Ö×ÓŹżÖ®±Č”¢øł¾Żm=nM”¢¦Ń=$\frac{M}{{V}_{m}}$¼ĘĖćÖŹĮ攢ĆܶČÖ®±Č£»
£Ø4£©øł¾Żc=$\frac{1000¦Ń¦Ų}{M}$¼ĘĖć³öøĆŃĪĖįµÄĪļÖŹµÄĮæÅØ¶Č£»Ļ”ŹĶ¹ż³ĢÖŠČÜÖŹµÄĪļÖŹµÄĮæ²»±ä£¬¾Ż“Ė¼ĘĖć³öĻ”ŹĶŗóŃĪĖįµÄÅØ¶Č£®
½ā“š ½ā£ŗ£Ø1£©4.9gĮņĖįµÄĪļÖŹµÄĮæŹĒ0.05mol£¬ĆæøöĮņĖį·Ö×ÓÖŠŗ¬ÓŠ2øöHŌ×Ó”¢4øöOŌ×Ó£¬Ōņ0.05molĮņĖį·Ö×ÓÖŠŗ¬ÓŠHŌ×ÓµÄĪļÖŹµÄĮæĪŖ£ŗ0.05mol”Į2=0.1mol£»ŗ¬ÓŠOŌ×ÓµÄĪļÖŹµÄĮæĪŖ0.05mol”Į4=0.2mol£¬øł¾ŻN=nNAÖŖ£¬ŗ¬ÓŠOŌ×ÓøöŹżĪŖ0.2NA£»
ĆæøöĖ®·Ö×ÓÖŠŗ¬ÓŠ1øöOŌ×Ó£¬ŌņĮņĖįŗĶĖ®ÖŠOŌ×ÓøöŹżĻąµČŹ±ĮņĖįŗĶĖ®µÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ4£¬Ė®µÄÖŹĮæm=nM=0.05mol”Į4”Į18g/mol=3.6g£¬
¹Ź“š°øĪŖ£ŗ0.1£»0.2NA£»3.6g£»
£Ø2£©±źæöĻĀ£¬44.8L¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæ=$\frac{44.8L}{22.4L/mol}$=2mol£¬m£ØCO2£©=nM=2mol”Į44g/mol=88g£»
Ćæøö·Ö×ÓÖŠŗ¬ÓŠÖŹ×ÓŹżŹĒ22£¬Ōņ2mol¶žŃõ»ÆĢ¼·Ö×ÓÖŠŗ¬ÓŠµÄÖŹ×ÓŹżŹĒ44NA£¬
¹Ź“š°øĪŖ£ŗ2mol£»88g£»44NA£»
£Ø3£©Ķ¬ĪĀĶ¬Ń¹ĻĀĘųĢåĦ¶ūĢå»żĻąµČ£¬ĻąĶ¬Ģå»żµÄCOŗĶ¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæĻąµČ£¬ĘäĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1£»øł¾ŻN=nNAÖŖ£¬ĻąĶ¬ĪļÖŹµÄĮæŹ±Ęä·Ö×ÓŹżĻąµČ£¬¶žÕß·Ö×ÓŹżÖ®±ČĪŖ1£ŗ1£»øł¾Żm=nMÖŖ£¬ĘäÖŹĮæÖ®±ČµČӌĦ¶ūÖŹĮæÖ®±Č=28g/mol£ŗ44g/mol=7£ŗ11£»øł¾Ż¦Ń=$\frac{M}{{V}_{m}}$æÉÖŖ£¬ĻąĶ¬Ģõ¼žĻĀĦ¶ūÖŹĮæÖ®±ČµČÓŚĘäĦ¶ūÖŹĮæÖ®±Č=28g/mol£ŗ44g/mol=7£ŗ11£¬
¹Ź“š°øĪŖ£ŗ1£ŗ1£»1£ŗ1£»7£ŗ11£»7£ŗ11£»
£Ø4£©ÖŹĮæ·ÖŹżĪŖ36.5%£¬ĆܶČĪŖ1.19g/mlµÄŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ£ŗc£ØHCl£©=$\frac{1000”Į1.19”Į36.5%}{36.5}$mol/L=11.9mol/L£»
Č”Ęä10mLĻ”ŹĶÖĮ100mL£¬Ļ”ŹĶ¹ż³ĢÖŠHClµÄĪļÖŹµÄĮæ²»±ä£¬ŌņĻ”ŹĶŗóµÄČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ£ŗ$\frac{11.9mol/L”Į0.01L}{0.1L}$=1.19mol/L£¬
¹Ź“š°øĪŖ£ŗ11.9£»1.19£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄĮæµÄÓŠ¹Ų¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·ĪļÖŹµÄĮ湫Ź½ÖŠø÷øöĪļĄķĮæÖ®¼ä¹ŲĻµŹĒ½ā±¾Ģā¹Ų¼ü£¬×¢ŅāĘųĢåĦ¶ūĢå»żŹŹÓĆ·¶Ī§¼°ŹŹÓĆĢõ¼ž£¬ŹŌĢāÅąŃųĮĖѧɜµÄ»Æѧ¼ĘĖćÄÜĮ¦£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 13.5g | B£® | 9g | C£® | 27g | D£® | 0.33mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”÷H=-1141.8kJ/mol | B£® | ”÷H=+260.4kJ/mol | ||
| C£® | ”÷H=+441.8kJ/mol | D£® | ”÷H=-260.4kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 92 | B£® | 143 | C£® | 235 | D£® | 327 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
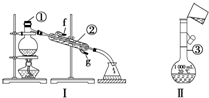 ÕĘĪÕŅĒĘ÷µÄĆū³Ę¼°Ź¹ÓĆ·½·ØŹĒ»ÆѧŹµŃéµÄ»ł“”£¬ČēĶ¼ĖłŹ¾ĪŖĮ½Ģ׏µŃé×°ÖĆ£®
ÕĘĪÕŅĒĘ÷µÄĆū³Ę¼°Ź¹ÓĆ·½·ØŹĒ»ÆѧŹµŃéµÄ»ł“”£¬ČēĶ¼ĖłŹ¾ĪŖĮ½Ģ׏µŃé×°ÖĆ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
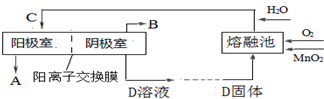
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ķ¬ĪĀ”¢Ķ¬Ń¹ĻĀ£¬ĻąĶ¬ÖŹĮæµÄĘųĢ嶼ռӊĻąĶ¬µÄĢå»ż | |
| B£® | Ķ¬ĪĀ”¢Ķ¬Ń¹ĻĀ£¬ĻąĶ¬Ģå»żµÄĘųĢ嶼ŗ¬ÓŠĻąĶ¬ŹżÄæµÄŌ×Ó | |
| C£® | ŌŚČĪŗĪĒéæöĻĀ£¬1 mol CO2ŗĶ64 g SO2Ėłŗ¬ÓŠ·Ö×ÓŹżŗĶŌ×Ó×ÜŹż¶¼ĻąĶ¬ | |
| D£® | 1 molijĘųĢåµÄĢå»żŌ¼ĪŖ22.4 L£¬øĆĘųĢåĖł“¦µÄדæöŅ»¶ØŹĒ±ź×¼×“æö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øśĖ®·“Ó¦Ź±£¬Ė®×÷Ńõ»Æ¼Į | B£® | NaHŌŚĖ®ÖŠĻŌĖįŠŌ | ||
| C£® | øśŅŗ°±·“Ó¦Ź±£¬ÓŠNaNH2Éś³É | D£® | øśŅŅ“¼·“Ó¦Ź±£¬NaH±»Ńõ»Æ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com