
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是
A. 0.5mol雄黄(As4S4),结构如右图,含有NA个S-S键![]()
B. 将1molNH4NO3溶于适量稀氨水中,所得溶液呈中性,则溶液中NH4+的数目为NA
C. 标准状况下,33.6L二氯甲烷中含有氯原子的数目为3NA
D. 高温下,16.8gFe与足量水蒸气完全反应,转移的电子数为0.6NA
科目:高中化学 来源: 题型:
【题目】如图装置所示,C、D、E、F、X、Y均为惰性电极,甲、乙中溶液体积均为500mL且溶液浓度均相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答:

(1)B极是电源的_____极,一段时间后,甲中溶液颜色逐渐变____,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明Fe(OH)3胶体微粒带____荷。
(2)电解一段时间后甲、乙装置中的C、D、E、F电极均分别只有一种单质生成时,对应单质的物质的量之比为______________,乙中发生反应的化学方程式为__________________________________,若要使电解后的甲装置中的溶液恢复到原浓度则需加入一定量的_________(填化学式)。
(3)现用丙装置给铜件镀银,则H应该是______(填“镀层金属”或“镀件”),当镀件上析出5.4g银时, 甲、乙中溶液的pH分别为_____和_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: 2NH4Cl(s)+ Ca(OH)2(s)![]() CaCl2(s)+2NH3↑+ 2H2O,现将107g NH4Cl晶体和111g熟石灰混合后,充分加热使之完全反应。求:
CaCl2(s)+2NH3↑+ 2H2O,现将107g NH4Cl晶体和111g熟石灰混合后,充分加热使之完全反应。求:
(1)产生的氨气在标准状况时的体积为多少?
(2)将所得氨气全部溶于200mL水中,若所得氨水的密度为0.936 g·cm-3,则该氨水的物质的量浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某蓄电池反应为NiO2+Fe+2H2O![]() Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
(1)该蓄电池充电时,发生还原反应的物质是 (填下列字母),放电时生成Fe(OH)2的质量18 g,则外电路中转移的电子数是 。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常把船体与浸在海水里的Zn块相连,或与该蓄电池这样的直流电源的 极(填“正”或“负”)相连。
(3)以该蓄电池做电源,用右图所示装置,在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示)。 。

(4)精炼铜时,粗铜应与直流电源的 极(填“正”或“负”)相连,精炼过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解,甲同学设计如下除杂方案:
![]()
已知:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
开始沉淀时的pH | 2.3 | 7.5 | 5.6 | 6.2 |
完全沉淀时的pH | 3.9 | 9.7 | 6.4 | 8.0 |
则加入H2O2的目的是 ,乙同学认为应将方案中的pH调节到8,你认为此观点 (填“正确”或“不正确”),理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素X、Y、Z、W原子序数依次增大,其中Y是构成物质种类最多的一种元素。m、n、p均为由这些元素组成的二元化合物,甲、乙、丙是其中三种元素对应的单质,m的自述是“诞生在闪电的弧光中,强大的能量造就了我”。n能使湿润的红色石蕊试纸变蓝。上述物质的转化关系如图所示(反应条件已略去)。下列说法正确的是

A. 常温常压下,X与Y组成的化合物一定为气体
B. X、Z、W三种元素不能组成离子化合物
C. 原子半径:X<W<Y<Z
D. 图示转化关系中涉及的反应均为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
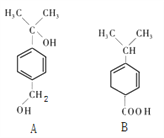
【题目】对下图两种化合物的结构或性质描述正确的是( )
①A、B的分子式均为C10H14O2它们互为同分异构体; 它们与分子式为C9H12O2的有机物一定为同系物
②A、B分子中共平面的碳原子数相同
③A、B均能使酸性高锰酸钾溶液褪色
④可用红外光谱区分,但不能用核磁共振氢谱区分A、B
⑤A、B都含有两种官能团
⑥1molA物质与足量金属钠反应与1molB与足量的饱和碳酸氢钠溶液反应生成气体的物质的量为2:1
⑦1molB与1molBr2发生加成反应能生成三种不同产物,且这三种产物互为同分异构体
A. ①②③④⑤⑥⑦ B. 只有③⑥⑦ C. 只有③ D. 只有③⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 醋酸溶解水垢:CH3COOH+CaCO3=CH3COO—+H2O+CO2
B. 在NH4Fe(SO4)2溶液中加入少量Ba(OH)2溶液:2Fe3+ + 3SO42-+ 3Ba2+ + 6OH-=== 3BaSO4↓+ 2Fe(OH)3↓
C. 氢氧化镁和盐酸反应:H++OH-===H2O
D. Ba(OH)2溶液中加入过量NH4HSO4溶液: Ba2++2OH-+NH4++H++SO42-=== BaSO4+NH3·H2O+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com