
| A、①⑤④③ | B、②③④③ |
| C、②③⑤③ | D、①⑤③ |


科目:高中化学 来源: 题型:
| A、C不一定是H2SO4 |
| B、物质的量浓度相等的A、B两溶液的pH大小关系:前者小于后者 |
| C、B溶于溴水中可生成沉淀 |
| D、若A、B两溶液的pH=9,则两溶液中由水电离出的OH-的物质的量浓度之比为1:104 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,将铁片置于浓硝酸中:Fe+6H++3NO3-═Fe3++3NO2↑+3H2O |
| B、向氯化铵的稀溶液中加入少量NaOH:NH4++OH-═NH3↑+H2O |
| C、向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-═BaSO4↓ |
| D、向浓硝酸中加入铜片:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钠中加入CaCl2溶液产生白色沉淀物 |
| B、硫酸铜溶液中插入铁片,铁片上出现红色沉淀物 |
| C、石灰石溶于盐酸并产生气泡 |
| D、氯化铵溶液中加入氢氧化钠溶液并加热,产生的气体使湿润的红石蕊试纸变蓝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
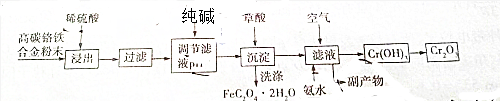
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、煤经过气化、液化等物理变化可得到清洁燃料 |
| B、棉花、羊毛、蚕丝都是由C、H、O元素构成 |
| C、食用冰糖和植物油的主要成分分别是蔗糖和甘油 |
| D、乙酸和乙酸乙酯可以用纯碱进行鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:
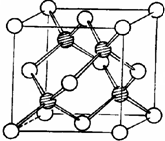 冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立方体内)类似.每个冰晶胞平均占有
冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立方体内)类似.每个冰晶胞平均占有查看答案和解析>>
科目:高中化学 来源: 题型:
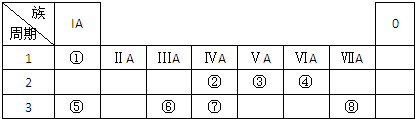
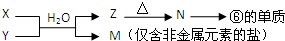 X溶液与Y溶液反应的离子方程式为
X溶液与Y溶液反应的离子方程式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烷和溴蒸气在光照下发生反应 |
| B、将乙烯通入溴水中发生反应 |
| C、乙烯与溴化氢在一定条件下反应 |
| D、乙炔与溴化氢在一定条件下反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com