
 �̷���FeSO4•7H2O��������ȱ����ƶѪ����Чҩ��ij��ѧ��ȤС����̷����������µ�̽����
�̷���FeSO4•7H2O��������ȱ����ƶѪ����Чҩ��ij��ѧ��ȤС����̷����������µ�̽�������� I������ͭ�������������ᷴӦ��������ͭ����������������������ͭ����������Ӧ��������������ͭ���ʣ�
��1��̼���Ƶ�ˮ��Һ�Լ��ԣ����Գ�ȥ��м��������ۣ�
��2��FeSO4�ױ�����������
��3������ͭ�������������ᷴӦ��������ͭ����������������������ͭ����������Ӧ��������������ͭ���ʣ�
��4�����ˣ���ȴ�ᾧ�ɵ�FeSO4•7H2O���壻
II����1������������Һ�IJ����Լ�ÿ��������Ҫ����ȷ����Ӧ����������
��2��������KMnO4��Һ��������ɫ��Ϊָʾ���жϵζ��յ㣻
��3��Fe2+��Fe3+����Ԫ�ػ��ϼ�����1�ۣ�MnO4-��Mn2+����Ԫ�ؽ���5�ۣ����ϼ�������С������Ϊ5�����ݹ�ϵʽ5Fe2+��MnO4-������25mL��Һ����Fe2+�����ʵ���������������Ʒ��FeSO4•7H2O���������ٸ�����������������㣻
��4������ʱ�������ƫ��
��� �⣺I����1��̼���Ƶ�ˮ��Һ�Լ��ԣ����Գ�ȥ��м��������ۣ��ʴ�Ϊ��ϴȥ��м��������ۣ�
��2��FeSO4�ױ���������������ͨ��N2�ų�װ���еĿ������������ʴ�Ϊ���ų�װ���еĿ�����������
��3������ͭ�������������ᷴӦ��������ͭ����������������������ͭ����������Ӧ��������������ͭ���ʣ��ʴ�Ϊ��Cu��
��4��ϴ�ӡ����ˡ���ȴ�ᾧ�ɵ�FeSO4•7H2O���壬�ʴ�Ϊ����ȴ���ᾧ��
II����1������Ϊ���������������Һ��ת�ơ�ϴ�ӡ����ݡ�ҡ�ȡ�װƿ����ǩ����Ҫʹ�õ������У�100mL ����ƿ��������ƽ���ձ�������������ͷ�ιܣ���Ͳ���ÿɲ��ã��ʴ�Ϊ��100mL ����ƿ����������
��2��������KMnO4��Һ��������ɫ��Ϊָʾ���жϵζ��յ�ʱ���ٵμ�KMnO4��Һʱ����Һ������ɫ��Ϊ�Ϻ�ɫ���ʴ�Ϊ�������һ�α�Һ����ʱ����Һ��Ϊ�Ϻ�ɫ����30s���ֲ��䣻
��3���ⶨ��Ʒ��Fe2+�ĺ���������������������KMnO4��Һ�ζ���Fe2+��Fe3+����Ԫ�ػ��ϼ�����1�ۣ�MnO4-��Mn2+����Ԫ�ؽ���5�ۣ����ϼ�������С������Ϊ5����Fe2+ϵ��Ϊ5��MnO4- ϵ��Ϊ1������Ԫ���غ��֪Mn2+��Fe3+ϵ���ֱ�Ϊ1��5�����ݵ���غ��֪ȱ��ΪH+��H+��ϵ��Ϊ2+3��5-[2��5-1]=8������HԪ���غ��֪H2Oϵ����4�����Է�Ӧ���ӷ���ʽΪ5Fe2++MnO4-+8H+=1Mn2++5Fe3++4H2O��
��Fe2+�����ʵ���Ϊxmol����
5Fe2+������������MnO4-��
5 1
xmol 0.01L��0.1mol/L
����x=$\frac{0.01��0.1mol/L��5}{1}$=0.005mol��
������Ʒ��FeSO4•7H2O������0.005mol��4��278g/mol=5.56g������4g��Ʒ��FeSO4•7H2O����������Ϊ$\frac{5.56g}{10g}$��100%=55.6%��
�ʴ�Ϊ��55.6%��
��4������ʱ�������ƫ��Ũ��ƫС���ʴ�Ϊ�����ӣ�
���� ���⿼�����ʵ��Ʊ��뺬���IJⶨ��Ϊ�߿��������ͺ�Ƶ���㣬������ѧ���ķ���������ʵ�������Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
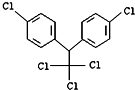
| A�� | �����ڷ����� | B�� | 1mol����������6mol H2�ӳ� | ||
| C�� | ����ʽΪC14H8Cl5 | D�� | ���л�������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 100 mL | B�� | 500 mL | C�� | 1000 mL | D�� | 1500 mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�¶� �ܽ�� ��ѧʽ | 20�� | 60�� | 100�� |
| Na2SO4 | 19.5 | 45.3 | 42.5 |
| Na2Cr2O7 | 183 | 269 | 415 |
| Na2CrO4 | 84 | 115 | 126 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
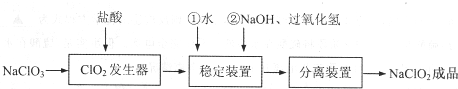
| ����� | ��ȡNaClO2��ƷWg����ˮ�����Һ������ƿ�У�������pH��2.0 |
| ����� | ����ƿ�м�������KI���壬��ֽ��裬����������ָʾ�� |
| ����� | ��c mol•L-1�� Na2S2O3��Һ�ζ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | 200��ʱ����Ӧ�ӿ�ʼ��ƽ���ƽ������v��B��=0.02 mol•L-1•min-1 | |
| B�� | ͼ����֪��ӦxA��g��+yB��g��?zC��g���ġ�H��0����a=2 | |
| C�� | ����ͼ����ʾ��ƽ��״̬�£�������ϵ�г���0.2molB��0.2molC�����´ﵽƽ��ǰv��������v���棩 | |
| D�� | ��200��ʱ���������г���2mol A ��1mol B���ﵽƽ��ʱ��A �������������0.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȥ���л��еı��ӿɼ���Ũ��ˮ����� | |
| B�� | �������Һ�еμ�ϡ������ȣ��ټ�������Cu��OH��2���ȣ�û�г��ֺ�ɫ������˵������û�з���ˮ�ⷴӦ | |
| C�� | ��NaOH��Һ�м��������飬���ȣ��ټ���AgNO3��Һ������������˵�������鷢����ˮ�ⷴӦ | |
| D�� | ������KMnO4��Һ�еμ�ά����C��Һ��KMnO4��Һ��ɫ��˵��ά����C�л�ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Σ�ջ�ѧƷ���Լ�ƿ��ǩ�����װ��һ�㶼�������ʶ | |
| B�� | �����κ��Լ����ɼ���AlCl3��Һ��NaOH��Һ | |
| C�� | ��ʹ����CuO��������һ����H2 | |
| D�� | �������ױ�����ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��� | B�� | ���� | ||
| C�� | ���ʵ���Ũ�� | D�� | H+��OH-�����ʵ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com