
·ÖĪö ¹ĢĢå»ģŗĻĪļæÉÄÜÓÉK2SO4”¢KI”¢NaCl”¢CuCl2”¢CaCl2ŗĶNa2CO3ÖŠµÄŅ»ÖÖ»ņ¼øÖÖ×é³É£¬
¢Ł»ģŗĻĪļ¼ÓĖ®µĆĪŽÉ«ĶøĆ÷ČÜŅŗ£¬ĖµĆ÷²»ŗ¬ÓŠÉ«Ąė×Ó£¬ŌņČÜŅŗÖŠŅ»¶Ø²»ŗ¬CuCl2£¬ĒŅĪļÖŹÖ®¼ä²»·“Ӧɜ³É³Įµķ£»
¢ŚĻņÉĻŹöČÜŅŗÖŠµĪ¼ÓBaCl2ČÜŅŗÓŠ°×É«³ĮµķÉś³É£¬½«øĆ³ĮµķĀĖ³ö£¬²¢½«ĀĖŅŗ·Ö³ÉĮ½·Ż£»
¢ŪÉĻŹö°×É«³ĮµķæÉĶźČ«ČÜÓŚĻ”ŃĪĖį£¬ĖµĆ÷°×É«³ĮµķµÄĢ¼Ėį±µ£¬ĖłŅŌČÜŅŗÖŠ²»ŗ¬K2SO4£¬ŗ¬ÓŠNa2CO3£¬øł¾ŻĄė×Ó¹²“ęÖŖ²»ŗ¬CaCl2£»
¢ÜĶłŅ»·ŻĀĖŅŗÖŠµĪ¼ÓĀČĖ®²¢¼ÓČėCCl4£¬Õńµ“ŗó¾²ÖĆ£¬CCl4²ć³ŹĪŽÉ«£¬ĖµĆ÷ČÜŅŗÖŠ²»ŗ¬KI£»
¢ŻĶłĮķŅ»·ŻĀĖŅŗÖŠ¼ÓČėAgNO3ČÜŅŗ£¬ÓŠ°×É«³ĮµķÉś³É£¬øĆ³Įµķ²»ČÜÓŚĻ”ĻõĖį£¬ŅņĪŖBaCl2ŗ¬ÓŠĀČĄė×Ó£¬ĖłŅŌ²»ÄÜČ·¶ØŌĄ“ČÜŅŗÖŠŹĒ·ńŗ¬ÓŠNaCl£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗ¹ĢĢå»ģŗĻĪļæÉÄÜÓÉK2SO4”¢KI”¢NaCl”¢CuCl2”¢CaCl2ŗĶNa2CO3ÖŠµÄŅ»ÖÖ»ņ¼øÖÖ×é³É£¬
¢Ł»ģŗĻĪļ¼ÓĖ®µĆĪŽÉ«ĶøĆ÷ČÜŅŗ£¬ĖµĆ÷²»ŗ¬ÓŠÉ«Ąė×Ó£¬ŌņČÜŅŗÖŠŅ»¶Ø²»ŗ¬CuCl2£¬ĒŅĪļÖŹÖ®¼ä²»·“Ӧɜ³É³Įµķ£»
¢ŚĻņÉĻŹöČÜŅŗÖŠµĪ¼ÓBaCl2ČÜŅŗÓŠ°×É«³ĮµķÉś³É£¬½«øĆ³ĮµķĀĖ³ö£¬²¢½«ĀĖŅŗ·Ö³ÉĮ½·Ż£»
¢ŪÉĻŹö°×É«³ĮµķæÉĶźČ«ČÜÓŚĻ”ŃĪĖį£¬ĖµĆ÷°×É«³ĮµķµÄĢ¼Ėį±µ£¬ĖłŅŌČÜŅŗÖŠ²»ŗ¬K2SO4£¬ŗ¬ÓŠNa2CO3£¬øł¾ŻĄė×Ó¹²“ęÖŖ²»ŗ¬CaCl2£»
¢ÜĶłŅ»·ŻĀĖŅŗÖŠµĪ¼ÓĀČĖ®²¢¼ÓČėCCl4£¬Õńµ“ŗó¾²ÖĆ£¬CCl4²ć³ŹĪŽÉ«£¬ĖµĆ÷ČÜŅŗÖŠ²»ŗ¬KI£»
¢ŻĶłĮķŅ»·ŻĀĖŅŗÖŠ¼ÓČėAgNO3ČÜŅŗ£¬ÓŠ°×É«³ĮµķÉś³É£¬øĆ³Įµķ²»ČÜÓŚĻ”ĻõĖį£¬ŅņĪŖBaCl2ŗ¬ÓŠĀČĄė×Ó£¬ĖłŅŌ²»ÄÜČ·¶ØŌĄ“ČÜŅŗÖŠŹĒ·ńŗ¬ÓŠNaCl£¬
£Ø1£©æÉŅŌÅŠ¶Ļ³ö»ģŗĻĪļÖŠæĻ¶Øŗ¬ÓŠNa2CO3£¬¹Ź“š°øĪŖ£ŗNa2CO3£»
£Ø2£©øł¾ŻŅŌÉĻ·ÖĪöÖŖ£¬»ģŗĻĪļÖŠæĻ¶Ø²»ŗ¬ÓŠK2SO4”¢KI”¢CuCl2”¢CaCl2£¬¹Ź“š°øĪŖ£ŗK2SO4”¢KI”¢CuCl2”¢CaCl2£»
£Ø3£©ĪŽ·ØČ·¶ØŹĒ·ńŗ¬ÓŠNaCl£¬ĪŖČ·Ö¤»ģŗĻĪļµÄ×é³É£¬»¹Šė×öĀČĄė×ӵļģŃ飬Ęä²Ł×÷·½·ØĪŖ£ŗ½«¹ĢĢåČÜÓŚĖ®£¬Č”ÉŁĮæČÜŅŗÓŚŹŌ¹ÜÖŠ£¬ĻņŹŌ¹ÜÖŠ¼ÓČėĻõĖįĖį»ÆµÄĻõĖįŅųČÜŅŗ£¬Čē¹ū²śÉś°×É«³Įµķ¾ĶĖµĆ÷ŗ¬ÓŠĀČ»ÆÄĘ£¬·ńŌņ²»ŗ¬ĀČ»ÆÄĘ£¬
¹Ź“š°øĪŖ£ŗĀČĄė×ӵļģŃ飬Ęä²Ł×÷·½·ØĪŖ£ŗ½«¹ĢĢåČÜÓŚĖ®£¬Č”ÉŁĮæČÜŅŗÓŚŹŌ¹ÜÖŠ£¬ĻņŹŌ¹ÜÖŠ¼ÓČėĻõĖįĖį»ÆµÄĻõĖįŅųČÜŅŗ£¬Čē¹ū²śÉś°×É«³Įµķ¾ĶĖµĆ÷ŗ¬ÓŠĀČ»ÆÄĘ£¬·ńŌņ²»ŗ¬ĀČ»ÆÄĘ£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹ¼ģŃ飬ĪŖøßĘµæ¼µć£¬Ć÷Č·ĪļÖŹŠŌÖŹ¼°ĪļÖŹÖ®¼ä·“Ó¦ŹĒ½ā±¾Ģā¹Ų¼ü£¬ÖŖµĄĀČĄė×Ó”¢ĮņĖįøłĄė×Ó”¢ļ§øłĄė×Ó”¢ŃĒĢśĄė×Ó”¢ĢśĄė×ӵȥė×ӵļģŃé·½·Ø¼°ĻÖĻó£¬ĢāÄæÄŃ¶Č²»“ó£®


 ±øÕ½ÖŠæ¼ŗ®¼ŁĻµĮŠ“š°ø
±øÕ½ÖŠæ¼ŗ®¼ŁĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¶žŃõ»ÆĢ¼ŹĒĪĀŹŅĘųĢ壬µ«²»ŹĒ“óĘųĪŪČ¾Īļ | |
| B£® | Å©“å³£ÓĆĆ÷·Æ¾»Ė®£¬ŹĒĄūÓĆĮĖ½ŗĢåµÄŠŌÖŹ | |
| C£® | Ź³Ę·Ģķ¼Ó¼Į¶ŌČĖĢåĪŽŗ¦£¬æÉ“óĮæŹ³ÓĆ | |
| D£® | ĀČ»ÆÄĘŹĒ³£ÓƵķĄøƼĮ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3ÖÖ | B£® | 4ÖÖ | C£® | 5ÖÖ | D£® | 6ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 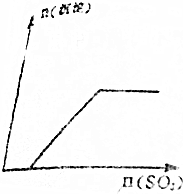 | B£® | 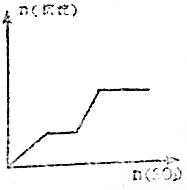 | ||
| C£® | 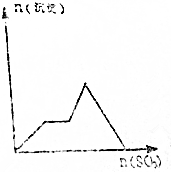 | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
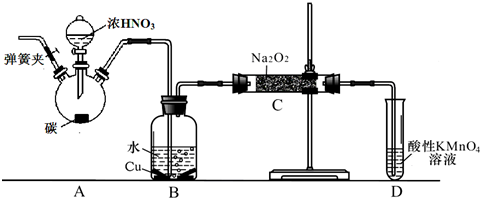
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
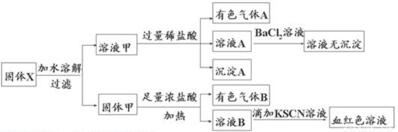
| A£® | ČÜŅŗ¼×ÖŠŅ»¶Øŗ¬ÓŠK2SO3”¢NaNO2 | B£® | ĪŽ·ØÅŠ¶ĻČÜŅŗÖŠŹĒ·ńÓŠK2SO3 | ||
| C£® | ĘųĢåAŗĶĘųĢåB-¶ØĪŖ»ģŗĻĪļ | D£® | Ō»ģŗĻĪļÖŠŅ»¶ØÓŠFe2O3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com