
| 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n(N2) | 0 | 0.20 | 0.35 | 0.40 | 0.40 |
| T2 | n(N2) | 0 | 0.25 | … | 0.30 | 0.30 |
| A. | T1温度下,CH4的平衡转化率为50% | |
| B. | T1<T2 | |
| C. | a<0 | |
| D. | T2时反应的平衡常数大于T1时反应的平衡常数 |
分析 A.由表中数据可知,40min处于平衡状态,平衡时生成氮气为0.4mol,根据方程式计算消耗甲烷物质的量,进而计算甲烷的转化率;
B.由前10min内,温度T2时生成氮气较多,说明温度T2的反应速率快,温度越高反应速率越快;
C.由B中分析可知,温度T1<T2,T2温度30min处于平衡状态,平衡时氮气的物质的量比T1温度小,说明升高温度平衡逆向移动;
D.升高温度平衡逆向移动,平衡常数减小.
解答 解:A.由表中数据可知,40min处于平衡状态,平衡时生成氮气为0.4mol,根据方程式可知消耗甲烷物质的量为0.4mol,则甲烷的转化率为$\frac{0.4mol}{0.5mol}$×100%=80%,故A错误;
B.由前10min内,温度T2时生成氮气较多,说明温度T2的反应速率快,温度越高反应速率越快,故温度T1<T2,故B正确;
C.由B中分析可知,温度T1<T2,T2温度30min处于平衡状态,平衡时氮气的物质的量比T1温度小,说明升高温度平衡逆向移动,则正反应为放热反应,故a<0,故C正确;
D.升高温度平衡逆向移动,平衡常数减小,T2时反应的平衡常数小于T1时反应的平衡常数,故D错误,
故选:AD.
点评 本题考查化学平衡计算及影响因素、平衡常数影响因素等,关键是根据数据判断温度大小,较好的考查学生对数据的分析处理能力,难度中等.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:解答题
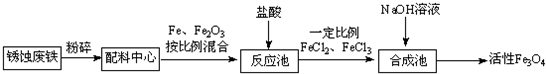
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
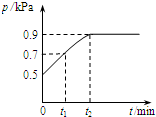 在1.0L密闭容器中放入0.1mol X,在一定温度下发生反应:X(g)?Y(g)+Z(g)△H<0 容器内气体总压强p随反应时间t的变化关系如图所示.以下分析正确的是( )
在1.0L密闭容器中放入0.1mol X,在一定温度下发生反应:X(g)?Y(g)+Z(g)△H<0 容器内气体总压强p随反应时间t的变化关系如图所示.以下分析正确的是( )| A. | t1时n(X)=0.04 mol | |
| B. | t1到t2,混合气体的平均相对分子量增大 | |
| C. | 欲提高平衡体系中Y的含量,可升高体系温度或减少Z的量 | |
| D. | 其他条件不变,再充入0.1 mol 气体X,平衡正向移动,X的转化率减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
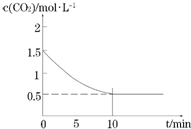 (1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1
(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
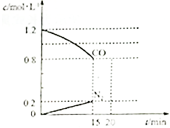 目前城市空气质量恶化原因之一是机动车尾气和燃煤产生的烟气,NO和CO均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:
目前城市空气质量恶化原因之一是机动车尾气和燃煤产生的烟气,NO和CO均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N3-:1s22s22p3 | B. | F-:1s22s22p6 | ||
| C. | Fe2+:1s22s22p63s23p63d6 | D. | O2-:1s22s22p6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因为SiO2是H2SiO3的酸酐,故SiO2溶于水得H2SiO3 | |
| B. | CO2通入水玻璃(Na2SiO3的水溶液)中可以得到硅酸沉淀 | |
| C. | 因为高温时发生反应:Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑,所以硅酸的酸性比碳酸强 | |
| D. | SiO2是酸性氧化物,它不溶于任何酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6mol | B. | 10mol | C. | 3amol | D. | 3mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com