
Ⅰ.现有八种微粒:Na、Mg2+ 、Fe2+、Fe3+、S2-、SO2、HCl、H2O,从元素化合价的角度分析,其中只有氧化性的是______ ,只有还原性的是_____ _,
既有氧化性又有还原性的是__________ _。
Ⅱ.已知能用氯酸钾与浓盐酸反应制取氯气,其化学方程式如下:
KClO3+6HCl =KCl+3Cl2↑+ 3H2O
⑴用单线桥在上述方程式中标出电子转移的方向和数目。
⑵标况下生成3.36LCl2,转移电子的物质的量为 ,被氧化的盐酸与未被氧化的盐酸质量之比为 。氧化产物与还原产物物质的量之比为 。
Fe3+,Mg2+(1分); Na, S2ˉ(1分); Fe2+,SO2,HCl,H2O(1分);
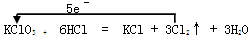 (线桥1分,电子数1分,共2分)
(线桥1分,电子数1分,共2分)
0.25mol(1分); 5:1(1分); 5:1(1分)
【解析】
试题分析::Ⅰ.Na, S2ˉ均为元素的最低价,则只具有还原性,
Fe3+,Mg2+均为元素的最高价,则只具有氧化性,
Fe2+,SO2,HCl,H2O处于中间价态元素的离子既有氧化性又有还原性。
Ⅱ.(1)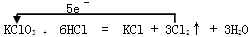
(2)标况下生成3.36LCl2,Cl2的物质的量为n=V/Vm =3.36L/(22.4L/mol)=0.15mol,则反应的HCl的物质的量为0.3mol,转移电子的物质的量为5/6×0.3mol=0.25mol;化合价升高和化合价未变的物质量之比为5:1,所以被氧化的盐酸与未被氧化的盐酸质量之比为5:1。氧化产物与还原产物物质的量之比为5:1。
考点:氧化还原反应;氧化还原反应的电子转移数目计算;氧化还原反应的计算.


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| ① | A1 | B1 | C1 | D1 |
| 电子数 | 10 | 10 | 10 | 18 |
| ② | A2 | B2 | C2 | D2 |
| 电子数 | 10 | 10 | 10 | 18 |
查看答案和解析>>
科目:高中化学 来源: 题型:
阳离子 | Na+、Mg2+、Al3+、Ba2+、 |
阴离子 | OH-、Cl-、 |
A、B、C、D、E是由它们组成的五种可溶于水的固体(每种离子只能用一次),分别取它们进行实验,结果如下:
①将D与E的溶液混合加热,产生有刺激性气味的气体
②将B与E的溶液混合,产生白色沉淀,向该沉淀中加入足量的稀硝酸,沉淀部分溶解
③向一定量的E溶液中逐滴加入C溶液,先无明显现象,后来产生白色沉淀,且该沉淀可溶于A溶液
④D固体在一定条件下可以分解为水和另外两种气体单质
(1)根据以上条件推断并写出下列物质的化学式:
A___________,B___________,C___________,D___________,E___________。
(2)写出A溶液与E溶液恰好完全反应至溶液呈中性的离子方程式:___________________。
(3)若
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)用A+、B-、C2―、D、E、F、G和H分别表示含有18个电子的八种微粒(离子或分子),请回答:
(1)A元素是 、B元素是 、C元素是 (用元素符号表示)。
(2)D是由两种元素组成的双原子分子,其分子式是 。
(3)E是所有含18个电子的微粒中氧化能力最强的分子,其分子式是 。
(4)F是由两种元素组成的三原子分子,其分子式是 ,结构式是 。
(5)G分子中含有4个原子,在MnO2催化作用下能生成一种无色无味的气体,该反应方程式为 。
(6)H分子中也含有4个原子,其分子式是 。该分子是 分子(填“极性”或“非极性”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com