
| n(SO32-):n(HSO3-) | 1:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
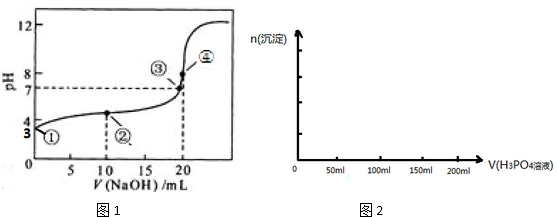
分析 (1)根据图象可知,起始①点溶液的pH为3,溶液中氢离子浓度为10-3mol/L,此时为0.1000mol/L的CH3COOH溶液,由于醋酸的电离程度较小,则醋酸根离子浓度约为10-3mol/L、醋酸的浓度约为0.1mol/L,将该数据代入醋酸的平衡常数表达式即可;
(2)由表中数据可知,溶液中n(SO32-):n(HSO3-)=1:1时,溶液pH=7.2,且比值越大,溶液的碱性越强,故吸收液呈中性时应n(SO32-):n(HSO3-)<1:1,溶液呈中性有c(H-)=c(OH-),结合电荷守恒有c(Na+)=2c(SO32-)+c(HSO3-),据此判断;
(3)液呈中性时,c(H+)=c(OH-),根据电荷守恒可知:c(Na+)+c(NH4+)=2c(SO32-),由于钠离子浓度大于亚硫酸根离子,则c(Na+)>c(SO32-)>c(NH4+);
(4)当加入$\frac{1}{15}$mol H3PO4时恰好生成Ca3(PO4)2,加入1mol•L-1的H3PO4溶液的体积为:$\frac{\frac{1}{15}mol}{1mol/L}$=0.067L=66.7mL;当加入0.1mol H3PO4时恰好生成CaHPO4,此时沉淀达到最大,消耗H3PO4溶液的体积为:$\frac{0.1mol}{1mol/L}$=0.1L=100mL;之后沉淀逐渐溶解,当加入0.1molH3PO4时沉淀完全溶解,消耗H3PO4溶液的体积为:$\frac{0.2mol}{1mol/L}$=0.2L=200mL,据此画出图象.
解答 解:(1)起始①点溶液的pH为3,此时为0.1000mol/L的CH3COOH溶液,溶液中氢离子浓度为10-3mol/L,醋酸根离子浓度约为10-3mol/L,醋酸的浓度约为0.1mol/L,则醋酸的电离平衡常数为:$\frac{1{0}^{-3}×1{0}^{-3}}{0.1}$=10-5,
故答案为:10-5;
(2)由表中数据可知,溶液中n(SO32-):n(HSO3-)=1:1时,溶液pH=7.2,且比值越大,溶液的碱性越强,故吸收液呈中性时应n(SO32-):n(HSO3-)<1:1,即c(HSO3-)>c(SO32-),溶液呈中性有c(H-)=c(OH-),结合电荷守恒推出c(Na+)=2c(SO32-)+c(HSO3-),故溶液中c(Na+)>c(HSO3-),所以溶液中c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-),
故答案为:c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-);
(3)向0.1mol•L的NaHSO3中通入氨气至溶液呈中性时,c(H+)=c(OH-),根据电荷守恒可知:c(Na+)+c(NH4+)=2c(SO32-),由于钠离子浓度大于亚硫酸根离子,则c(Na+)>c(SO32-)>c(NH4+),所以溶液中c(H+)、c(OH-)、c(SO32-)、c(Na+)、c(NH4+)这五种离子浓度大小关系为:c(Na+)>c(SO32-)>c(NH4+)>c(H+)=c(OH-),
故答案为:c(Na+)>c(SO32-)>c(NH4+)>c(H+)=c(OH-);
(4)在含0.1mol Ca(OH)2的澄清石灰水中逐渐加入1mol•L-1的H3PO4,当加入$\frac{1}{15}$mol H3PO4时恰好生成Ca3(PO4)2,加入1mol•L-1的H3PO4溶液的体积为:$\frac{\frac{1}{15}mol}{1mol/L}$=0.067L=66.7mL;当加入0.1mol H3PO4时恰好生成CaHPO4,此时沉淀达到最大,消耗H3PO4溶液的体积为:$\frac{0.1mol}{1mol/L}$=0.1L=100mL;之后沉淀逐渐溶解,当加入0.1molH3PO4时沉淀完全溶解,消耗H3PO4溶液的体积为:$\frac{0.2mol}{1mol/L}$=0.2L=200mL,据此画出成沉淀的物质的量随H3PO4滴入体积从0开始至200mL的图象为: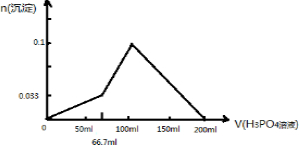 ,
,
故答案为: .
.
点评 本题考查了离子浓度大小比较,题目难度中等,涉及电离平衡常数的计算、离子浓度大小比较及绘画反应图象等知识,注意掌握电离平衡常数的概念及计算方法,明确电荷守恒、盐的水解原理、物料守恒在判断离子浓度大小中的应用方法.


 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源: 题型:选择题

| A. | X为氧气 | |
| B. | 电极A反应式:CH3CH2OH-12e-+3H2O═2CO2+12H+ | |
| C. | 电极材料活泼性:A>B | |
| D. | B电极附近溶液pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
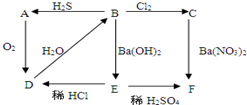 图中A为淡黄色固体,B、C为溶液,D为气体,E、F为白色沉淀.
图中A为淡黄色固体,B、C为溶液,D为气体,E、F为白色沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
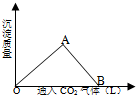 (1)在模拟溶洞的“形成”实验中,将过量二氧化碳气体通入饱和Ca(OH)2溶液中,产生CaCO3白色沉淀的质量与通入的二氧化碳气体体积之间的关系曲线如图所示.
(1)在模拟溶洞的“形成”实验中,将过量二氧化碳气体通入饱和Ca(OH)2溶液中,产生CaCO3白色沉淀的质量与通入的二氧化碳气体体积之间的关系曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.015 | 0.012 | 0.010 | 0.010 | 0.010 |
| A. | 在0~2s内,v(O2)=0.002mol•L-1•s-1 | |
| B. | 5s后向容器中通入0.02mol NO2,再次平衡后,0.020mol<n(NO2)<0.040 mol | |
| C. | 在该温度时,向容器中加入O2,平衡将正向移动,平衡常数增大 | |
| D. | 5s后,向反应容器中同时通入各0.01mol的NO、O2、NO2,平衡向正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Cl-、NO3-、K+ | B. | HCO3-、K+、SO4 2-、Cl- | ||
| C. | Fe2+、Cl-、Na+、NO3- | D. | Ba2+、Cl-、K+、SO4 2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(NO3)2 溶液 | B. | AgNO3 溶液 | C. | Ba(OH)2 溶液 | D. | NaOH 溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
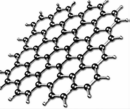 | 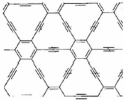 |  |
| 石墨烯:从石墨中分离出来,是最薄、最坚硬的物质 | 石墨块:平面网状结构的全碳分子,具有优良的化学稳定性 | 纳米碳管:具有优良的场发射性能,制作阴极显像管、储氢材料 |
| A. | 石墨烯具有良好的导电性 | |
| B. | 上述三种物质与金刚石互为同素异形体 | |
| C. | 石墨炔孔径略大于H2分子的直径,可作H2的提纯薄膜 | |
| D. | 上述三种物质与浓硫酸都能发生反应,但反应产物不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com