
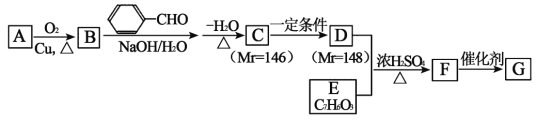
【题目】有机高分子化合物G的合成路线如图:(部分产物及反应条件已略去)
已知:①2RCH2CHO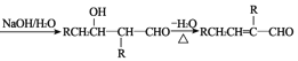
②E遇FeCl3溶液呈紫色,且能与NaHCO3溶液反应生成无色气体,其核磁共振氢谱有4组吸收峰。
回答下列问题:
(1)A的名称为___,G的结构简式为___。
(2)A→B的化学方程式为___,该反应的类型为___。
(3)C发生银镜反应的化学方程式为___。
(4)D+E→F的化学方程式为___。
(5)H为D的同分异构体,且H分子中含有(![]() ),苯环上有2个取代基,则H的可能结构有___种(不考虑立体异构),其中,能与新制氢氧化铜悬浊液反应产生砖红色沉淀且核磁共振氢谱有5组吸收峰的结构简式为___。
),苯环上有2个取代基,则H的可能结构有___种(不考虑立体异构),其中,能与新制氢氧化铜悬浊液反应产生砖红色沉淀且核磁共振氢谱有5组吸收峰的结构简式为___。
【答案】丙醇(或1-丙醇) 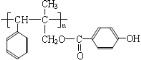 2CH3CH2CH2OH+O2
2CH3CH2CH2OH+O2![]() 2CH3CH2CHO+2H2O 氧化反应
2CH3CH2CHO+2H2O 氧化反应 ![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
![]() +2Ag↓+3NH3+H2O
+2Ag↓+3NH3+H2O ![]() +
+![]()
![]()
![]() +H2O 24
+H2O 24 ![]()
【解析】
由已知信息①和图中转化关系可推知,B分子中含有醛基(-CHO),且Mr(B)+Mr(![]() )-Mr(H2O)=Mr(C)=146,则Mr(B)=58,故B的结构简式为CH3CH2CHO,进而推知A为CH3CH2CH2OH。结合信息①可推知,C为
)-Mr(H2O)=Mr(C)=146,则Mr(B)=58,故B的结构简式为CH3CH2CHO,进而推知A为CH3CH2CH2OH。结合信息①可推知,C为![]() 。由已知信息②可知,E分子中含有酚羟基(-OH)和羧基(-COOH),且分子中有4种不同的氢原子,则苯环上只有2种不同的氢原子,即酚羟基和羧基处于苯环的对位,E为
。由已知信息②可知,E分子中含有酚羟基(-OH)和羧基(-COOH),且分子中有4种不同的氢原子,则苯环上只有2种不同的氢原子,即酚羟基和羧基处于苯环的对位,E为![]() 。D能与E发生酯化反应,说明D中含有羟基,比较C和D的相对分子质量可知,C分子中的醛基与H2发生了加成反应而碳碳双键并没有发生加成反应,故D为
。D能与E发生酯化反应,说明D中含有羟基,比较C和D的相对分子质量可知,C分子中的醛基与H2发生了加成反应而碳碳双键并没有发生加成反应,故D为![]() ,进而推知,F为
,进而推知,F为![]() ,F可以通过加聚反应生成G,则G为
,F可以通过加聚反应生成G,则G为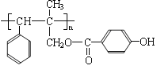 。
。
(1)由上面的分析可知A为丙醇(或1-丙醇)。G的结构简式为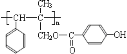 。答案为:丙醇(或1-丙醇);
。答案为:丙醇(或1-丙醇); ![]() ;
;
(2)A在催化剂Cu和加热条件下,被氧气氧化为B,反应的化学方程式为:2CH3CH2CH2OH+O2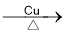 2CH3CH2CHO+2H2O,该反应为氧化反应。答案为:氧化反应;
2CH3CH2CHO+2H2O,该反应为氧化反应。答案为:氧化反应;
(3)C分子含有醛基,能发生银镜反应,反应方程式为:![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
![]() +2Ag↓+3NH3+H2O。答案为:
+2Ag↓+3NH3+H2O。答案为:![]() +2Ag(NH3)2OH
+2Ag(NH3)2OH![]()
![]() +2Ag↓+3NH3+H2O;
+2Ag↓+3NH3+H2O;
(4)D和E发生酯化反应,化学方程式为:![]() +
+![]()
![]()
![]() +H2O。答案为:
+H2O。答案为:![]() +
+![]()
![]()
![]() +H2O;
+H2O;
(5)H为D(![]() )的同分异构体,且H分子中含有(
)的同分异构体,且H分子中含有(![]() ),苯环上有2个取代基,结合D的结构简式可知,H分子中的2个取代基可以是烷基和醛基或烷基和羰基,共有8组:—CHO、—CH2CH2CH3,—CHO、—CH(CH3)2,—CH2CHO、—CH2CH3,—CH2CH2CHO、—CH3,—CH(CH3)CHO、—CH3,
),苯环上有2个取代基,结合D的结构简式可知,H分子中的2个取代基可以是烷基和醛基或烷基和羰基,共有8组:—CHO、—CH2CH2CH3,—CHO、—CH(CH3)2,—CH2CHO、—CH2CH3,—CH2CH2CHO、—CH3,—CH(CH3)CHO、—CH3,![]() 、—CH2CH3,
、—CH2CH3,![]() 、—CH3,
、—CH3,![]() 、—CH3,每组取代基在苯环上的位置可以分别为邻、间、对3种,故H的结构简式的种数=3×8=24。其中,能与新制氢氧化铜悬浊液反应产生砖红色沉淀,说明分子中含有醛基,且核磁共振氢谱有5组吸收峰的结构简式为
、—CH3,每组取代基在苯环上的位置可以分别为邻、间、对3种,故H的结构简式的种数=3×8=24。其中,能与新制氢氧化铜悬浊液反应产生砖红色沉淀,说明分子中含有醛基,且核磁共振氢谱有5组吸收峰的结构简式为![]() 。答案为:24;
。答案为:24;![]() 。
。


科目:高中化学 来源: 题型:
【题目】室温下,向20.00 mL 0.1000 mol·L1盐酸中滴加0.1000 mol·L1 NaOH溶液,溶液的pH随NaOH溶液体积的变化如图,已知lg3=0.5。下列说法不正确的是
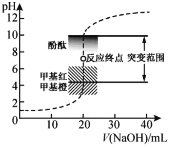
A.选择变色范围在pH突变范围内的指示剂,可减小实验误差
B.用移液管量取20.00 mL 0.1000 mol·L1盐酸时,移液管水洗后需用待取液润洗
C.NaOH标准溶液浓度的准确性直接影响分析结果的可靠性,因此需用邻苯二甲酸氢钾标定NaOH溶液的浓度,标定时采用甲基橙为指示剂
D.V(NaOH)=10.00 mL 时,pH约为1.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组在实验室从海带中提取碘,设计实验流程如下:
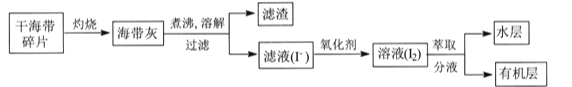
下列说法错误的是
A.过滤操作主要除去海带灰中难溶于水的固体,它们主要是无机物
B.氧化剂参加反应的离子方程式为2I-+H2O2+2H+=I2+2H2O
C.萃取过程所用有机溶剂可以是酒精或四氯化碳
D.因I2易升华,I2的有机溶液难以通过蒸馏法彻底分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物R的结构简式如图,下面有关说法不正确的是( )

A.1molR与足量的Na反应能生成1molH2
B.1molR最多能消耗2molNaOH
C.R能发生取代反应、加成反应、氧化反应、还原反应等反应类型
D.1molR完全燃烧消耗16molO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了①~⑨九种元素在周期表中的位置.
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ||||||
4 | ⑧ | ⑨ |
请按要求回答下列问题.
(1)这九种元素中,原子半径最大的是(填元素符号)__;元素⑤的原子结构示意图为___.
(2)③、④、⑤三种元素的气态氢化物中,热稳定性最弱的物质是(填化学式)______.
(3)写出元素⑧的单质与水反应的化学方程式:______.
(4)写出元素⑦的单质与元素⑨的钠盐溶液反应的离子方程式:______.
查看答案和解析>>
科目:高中化学 来源: 题型:
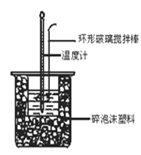
【题目】下列有关中和热概念、中和热测定实验(如图)的说法正确的是
A.已知在稀溶液中:H+(aq)+OH-(aq) =H2O(l);ΔH=-57.3kJ·mol-1,则有![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)=
Ba(OH)2(aq)= ![]() BaSO4(s)+H2O(l) △H=-57.3kJ·mol-1
BaSO4(s)+H2O(l) △H=-57.3kJ·mol-1
B.已知2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-114.6kJ·mol-1,则该反应的中和热为114.6 kJ·mol-1。
C.中和热测定实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小
D.酸碱混合时,量筒中的NaOH溶液应分多次倒入已装有盐酸的小烧杯中,并不断用环形玻璃搅拌棒搅拌。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中,可逆反应N2(g)+3H2(g)![]() 2NH3(g),达到平衡的标志是
2NH3(g),达到平衡的标志是
①反应速率v(N2)∶v(H2)∶v(NH3)=1∶3∶2;②各组分的物质的量浓度不再改变;③体系的压强不变;④混合气体的密度不变 (相同状况);⑤体系的温度不再发生变化;⑥2 v(N2)(正)=v(NH3)(逆) ;⑦单位时间内有3mol H—H断裂同时有2mol N—H断裂。
A.①②③⑤⑥⑦B.②③④⑤⑥C.②③⑤⑥D.②③④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.已知2A2(g)+B2(g)![]() 2C(g) ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
2C(g) ΔH=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol/L,放出热量b kJ。
(1)a________b(填“>”“=”或“<”)。
(2)若将反应温度升高到700 ℃,该反应的平衡常数将________(填“增大”“减小”或“不变”)。
(3)若在原来的容器中,只加入2 mol C,500 ℃时充分反应达到平衡后, C的浓度________w mol/L(填“>”“=”或“<”)
(4)使该反应的反应速率增大,且平衡向正反应方向移动的操作是________。
a.及时分离出C气体 b.适当升高温度
c.增大B2的浓度 d.选择高效的催化剂
II.氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g)![]() Si3N4(s)+ 6CO(g) △H>0 。
Si3N4(s)+ 6CO(g) △H>0 。
(1)该反应的平衡常数表达式为__________。
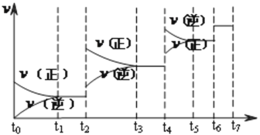
(2)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率![]() 与时间t的关系如下图。图中t3时引起平衡移动的条件可以是____________________;t4时引起平衡移动的条件可以是____________________;图中表示平衡混合物中CO的含量最高的一段时间是_________。
与时间t的关系如下图。图中t3时引起平衡移动的条件可以是____________________;t4时引起平衡移动的条件可以是____________________;图中表示平衡混合物中CO的含量最高的一段时间是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种晶体的晶胞结构如图所示,下列有关说法正确的是( )
A.图甲所示晶体的化学式为A3B4C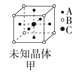
B.图乙所示晶体中阴阳离子个数比为1:1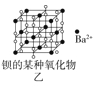
C.图丙所示CaF2晶体中Ca2+配位数为4,F-配位数为8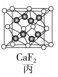
D.图丁所示晶体属于简单立方堆积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com