
| A、①③⑤⑥ | B、①②③④ |
| C、③④⑤⑥ | D、①②③④⑤⑥ |


科目:高中化学 来源: 题型:
| A、用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 |
| B、用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
| C、用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl 溶液全部蒸干才停止加热 |
| D、Hg(NO3)2溶于水,可将含有Hg(NO3)2的废液倒入水池中,再用水冲入下水道 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碱性氢氧燃料电池的正极反应式为:H2+2OH--2e-═2H2O |
| B、用铂电极电解硫酸铜溶液的阳极反应式为:2H2O-4e-═O2↑+4H+ |
| C、醋酸与稀NaOH溶液反应的热化学方程式为:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ?mol-1 |
| D、NaHSO3溶于水时水解的离子方程式为:HSO3-+H2O?SO32-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 甘油三酯 0.52 mmol/L 总胆固醇 4.27 mmol/L 高密度脂蛋白胆固醇 1.57 mmol/L 低密度脂蛋白胆固醇 1.40 mmol/L 葡萄糖 4.95 mmol/L |
| A、溶解度 | B、物质的量浓度 |
| C、质量分数 | D、摩尔质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③ | B、①③ | C、① | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 国家“十二五规划”明确提出了节能减排的目标,“节能减排”的含义就是节约能源、降低能源消耗、减少污染物排放.合成氨反应放出的热量可用于供暖和发电,是节能的有效措施之一.请你结合学过的知识回答下列问题:
国家“十二五规划”明确提出了节能减排的目标,“节能减排”的含义就是节约能源、降低能源消耗、减少污染物排放.合成氨反应放出的热量可用于供暖和发电,是节能的有效措施之一.请你结合学过的知识回答下列问题:| 时间/min | CH4(mol) | H2O(mol) | CO(mol) | H2(mol) |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | 0.20 | 0.80 | 0.20 | a |
| 7 | 0.20 | 0.80 | 0.20 | a |
| 10 | 0.21 | 0.81 | 0.19 | 0.64 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+、Na+、SO42-、Cl- |
| B、K+、Na+、HCO3-、NO3- |
| C、H+、CO32-、Ca2+、Na+ |
| D、Ba2+、Na+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、苯酚钠溶液中通入二氧化碳:2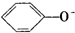 +CO2+H2O→CO32-+2 +CO2+H2O→CO32-+2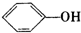 |
| B、醋酸溶液中加入氢氧化钠溶液:H++OH-═H2O |
| C、向Mg(HCO3)2溶液中加入过量的NaOH溶液:Mg2++2HCO3-+4OH-═Mg(OH)2↓+2CO32-+2H2O |
| D、碳酸氢钠溶液呈碱性:HCO3-+H2O?CO32-+H3O+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com