
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1076 | 465 | 413 |
分析 (1)在常温常压下,“可燃冰”会发生分解反应生成甲烷与水;
(2)①在101kPa时,1.6g CH4 (g)与H2O(g)反应生成CO、H2,吸热20.64kJ,则1mol甲烷反应吸收热量为206.4kJ,注明物质的聚集状态与反应热书写热化学方程式;
②CH4不完全燃烧制合成气时,放出热量,同时得到的CO、H2的化学计量数之比为1:2,能恰好完全反应合成甲醇;
(3)反应热=反应物总键能-生成物总键能;根据盖斯定律:反应②-反应①=反应③,反应热也进行相应的计算;
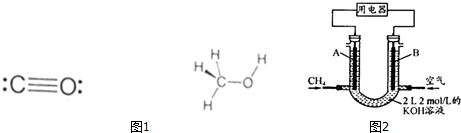
(4)可燃冰中CH4的其它用途是燃料;n(KOH)=2mol/L×2L=4mol,该装置是燃料电池,负极上甲烷失电子发生氧化反应,正极上氧气得电子发生还原反应,根据原子守恒得2mol<n(CO2)≤4mol,反应生成碳酸氢钾.
解答 解:(1)在常温常压下,“可燃冰”会发生分解反应生成甲烷与水,反应方程式为:CH4•nH2O=CH4↑+nH2O,
故答案为:CH4•nH2O=CH4↑+nH2O;
(2)①在101kPa时,1.6g CH4 (g)与H2O(g)反应生成CO、H2,吸热20.64kJ,则1mol甲烷反应吸收热量为206.4kJ,热化学方程式为CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.4 kJ•mol-1;
故答案为:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.4 kJ•mol-1;
②CH4不完全燃烧制合成气时,放出热量,同时得到的CO、H2的化学计量数之比为1:2,能恰好完全反应合成甲醇,而方法一吸收热量,得到CO、H2的化学计量数之比为1:3,不能恰好转化为甲醇,故方法二更好,
故答案为:②;
(3)反应热=反应物总键能-生成物总键能,故△H1=1076kJ.mol-1+2×436kJ.mol-1-(3×413+343+465)kJ.mol-1=-99kJ.mol-1;
根据盖斯定律:反应②-反应①=反应③,故△H3=△H2-△H1=-58kJ.mol-1-(-99kJ.mol-1)=+41kJ.mol-1,
故答案为:-99;+41;
(4)可燃冰中CH4的其它用途是燃料;n(KOH)=2mol/L×2L=4mol,该装置是燃料电池,负极上甲烷失电子发生氧化反应,正极上氧气得电子发生还原反应,44.8L<V≤89.6L时,根据原子守恒得2mol<n(CO2)≤4mol,反应生成碳酸氢钾,负极反应式为CH4-8e-+9CO32-+3H2O=10HCO3-,
故答案为:能源和燃料;CH4-8e-+9CO32-+3H2O=10HCO3-.
点评 本题考查反应热有关计算、实验方案的评价和电极反应的书写等,侧重考查学生分析计算能力,需要学生具备扎实的基础,难度中等.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 摩尔质量就等于物质的式量 | |
| B. | 摩尔质量就是物质式量的6.02×1023倍 | |
| C. | HNO3的摩尔质量是63g | |
| D. | 硫酸和磷酸的摩尔质量相等,都是98g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去NaHCO3溶液中少量的Na2CO3:通入过量的CO2 | |
| B. | 胶体是一种能产生丁达尔效应的分散系 | |
| C. | 纯碱不属于碱,干冰属于酸性氧化物 | |
| D. | Na2O和Na2O2都能与水反应生成对应的碱,它们都是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 塑料、合成橡胶和合成纤维是三大合成材料 | |
| B. | 在聚乙烯中,-CH2-CH2-称为单体 | |
| C. | 通过加聚反应得到涤纶、环氧树脂、酚醛树脂 | |
| D. | 通过缩聚反应得到聚丙烯、聚甲基丙烯酸甲酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称取3.2gNaCl固体 | |
| B. | 用10mL量筒量取7.50mL稀盐酸 | |
| C. | 用450mL的容量瓶配制450mL溶液 | |
| D. | 用广泛pH试纸测得某溶液的pH为3.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠与水反应 | B. | 氧化钠和水反应 | ||
| C. | 过氧化钠和水反应 | D. | 碳酸钠与水和二氧化碳反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验事实 | 理论解释 |
| A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
| B | 足球烯(C60)在苯中的溶解度大 | 足球烯是原子晶体 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com