
 MnCO3↓+CO2↑+H2O(2分)
MnCO3↓+CO2↑+H2O(2分) ×100%=90%(1分)
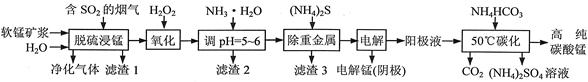
×100%=90%(1分) MnCO3↓+CO2↑+H2O;电解时溶液中产生氢离子溶液为酸性,会溶解碳酸盐,故加入过量碳酸氢铵反应调节溶液酸碱性,防止MnCO3沉淀溶解损失;碳酸氢铵不稳定受热易分解,故需多加试剂弥补分解损失。
MnCO3↓+CO2↑+H2O;电解时溶液中产生氢离子溶液为酸性,会溶解碳酸盐,故加入过量碳酸氢铵反应调节溶液酸碱性,防止MnCO3沉淀溶解损失;碳酸氢铵不稳定受热易分解,故需多加试剂弥补分解损失。

科目:高中化学 来源:不详 题型:实验题
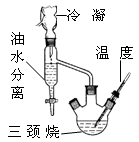
| 物 质 | 水 | 乙醇 | 乳酸 | 苯 | 乳酸乙酯 |
| 沸点/℃ | 100 | 78.4 | 122 | 80.10 | 154 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
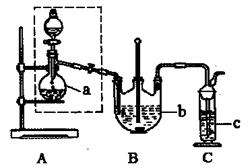
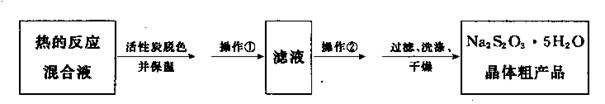
| A.用碱式滴定管盛装碘标准溶液 |
| B.用移液管移取25.00mL溶液于锥形瓶中,移液管的尖嘴和锥形瓶内壁要接触 |
| C.如果滴定终点没有控制好,碘标准溶液滴加过量,则必须重新进行滴定 |
| D.滴定过程中若剧烈摇动锥形瓶(溶液不外溅),则所测得的纯度将会偏高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| B.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
| C.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- |
| D.加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作及现象 | 实验目的或结论 |
| A | 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 可证明氧化性:H2O2比Fe3+强 |
| B | 在0.1 mol·L-1的NaHCO3溶液中,加2滴酚酞显浅红色,微热,溶液颜色加深 | 验证盐类水解反应是吸热反应 |
| C | 将一定量的NaNO3和KCl的混合液加热并 浓缩至有晶体析出时,趁热过滤 | 得到NaCl晶体 |
| D | 苯酚钠溶液中通入足量二氧化碳产生浑浊 | 苯酚的酸性弱于碳酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 混合物 | 试剂 | 分离方法 |
| A | 乙烯(二氧化硫) | 溴水 | 洗气 |
| B | 溴苯(溴) | NaOH溶液 | 分液 |
| C | 苯(苯酚) | 加浓溴水 | 过滤 |
| D | 乙烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
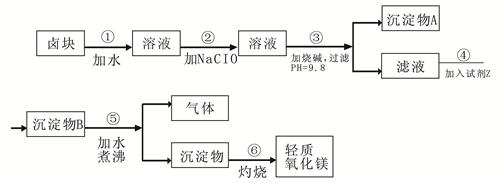
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
| 试剂 | 价格(元/吨) |
| 漂液(含NaClO,25.2%) | 450 |
| 双氧水(含H2O2 ,30%) | 2400 |
| 烧碱(含98% NaOH) | 2100 |
| 纯碱(含99.5% Na2CO3) | 600 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com