
 日本一家公司日前宣布,他们已经开发并计划大量生产一种颠覆性的阳极和阴极都是碳材料的双碳性电池(放电原理示意如图所示),充电速度比普通的锂离子电池快20倍.放电时,正极反应Cn(PF6)+e-═PF6-+nC,负极反应LiCn-e-═Li++nC下列有关说法中正确的是( )
日本一家公司日前宣布,他们已经开发并计划大量生产一种颠覆性的阳极和阴极都是碳材料的双碳性电池(放电原理示意如图所示),充电速度比普通的锂离子电池快20倍.放电时,正极反应Cn(PF6)+e-═PF6-+nC,负极反应LiCn-e-═Li++nC下列有关说法中正确的是( )| A. | a极为电池的负极 | |
| B. | A-为OH- | |
| C. | 电池充电时阴极反应为:LiCn+e-═Li++nC | |
| D. | 充电时,溶液中A-从b极向a极迁移 |
分析 A、根据原电池中电解质中的阴离子移向负极,阳离子移向正极来回答;
B、根据金属锂可以和水溶液之间反应来判断;
C、电池充电时是电解装置原理,阴极上发生得电子的还原反应,据此书写电极反应;
D、充电时,是电解装置原理,溶液中阴离子移向阳极,据此回答.
解答 解:A、原电池中电解质中的阴离子移向负极,阳离子移向正极,a电极是正极,故A错误;
B、金属锂可以和水溶液之间反应,电解质不是强电解质的水溶液,所以阴离子不能为OH-,故B错误;
C、电池充电时是电解装置原理,阴极上发生得电子的还原反应,和负极反应互为逆反应,电极反应为:Li++nC-e-=LiCn,故C错误;
D、充电时,是电解装置原理,溶液中阴离子移向阳极,即从b极向a极迁移,故D正确.
故选D.
点评 本题考查学生原电池、电解池的工作原理等知识,属于综合知识的考查,注意电极反应的书写是重点,难度不大.


科目:高中化学 来源: 题型:选择题
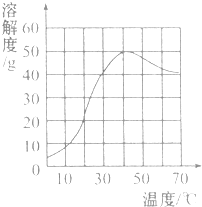
| A. | 硫酸钠的溶解度随温度升高而增大 | |
| B. | 30℃时硫酸钠饱和溶液的质量分数为40% | |
| C. | 40℃时硫酸钠的溶解度约为50g | |
| D. | 60℃时硫酸钠饱和溶液降温后一定饱和 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:A<B<C<D<E | |
| B. | 化合物AE与CE含有相同类型的化学键 | |
| C. | 金属性:D>C | |
| D. | 一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌粒与稀醋酸反应:Zn+2H+=Zn2++H2↑ | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42ˉ=BaSO4↓ | |
| C. | 氯化铝溶液与过量氨水反应:Al3++3OH-=Al(OH)3↓ | |
| D. | 常温下,用氢氧化钠溶液吸收多余的氯气:Cl2+2OH-=Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤经过气化和液化两个物理变化,可变为清洁能源 | |
| B. | 新型生物柴油和矿物油主要化学成分相同 | |
| C. | “洁厕灵”有效成分为盐酸,与漂白粉混合使用效果更佳 | |
| D. | 用银器盛放鲜牛奶,溶入的极微量的银离子,可杀死牛奶中的细菌,防止牛奶变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
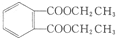 )是一种重要的工业塑化剂,其合成路线很多,如图就是其中的一种合成方法:
)是一种重要的工业塑化剂,其合成路线很多,如图就是其中的一种合成方法: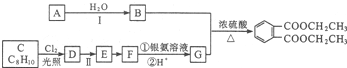
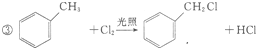
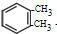 +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$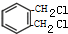 +2HCl.
+2HCl.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L0.1mol/L NaHCO3溶液中含有0.1NA个HCO${\;}_{3}^{-}$ | |
| B. | 78gNa2O2与足量CO2反应,转移电子数为NA | |
| C. | 100℃时,1L pH=1的硫酸溶液中,含有0.05NA个SO42- | |
| D. | 常温常压下,4g CH4含NA个共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 KHC2O4溶液中:c(OH-)=c(H+)+c(H2C2O4)-c(C2O42-) | |
| B. | pH相等的①CH3COONa、②C6H5ONa、③Na2CO3、④NaOH四种溶液的物质的量浓度大小:①>②>③>④ | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) | |
| D. | 向0.1 mol•L-1 NH4HSO4溶液中滴加NaOH至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使pH试纸呈红色的溶液中可能大量存在以下离子:Na+、NH4+、I-、NO3- | |
| B. | 将CH3COOH溶液和NaOH溶液等体积混合,该溶液中一定存在的关系式为:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | pH=3的NaHA溶液中粒子浓度大小为:c(Na+)>c(HA-)>c(A2-)>c(H2A)>c(OH-) | |
| D. | CuSO4溶液遇到闪锌矿(ZnS)慢慢转化为铜蓝(CuS),是因为ZnS的溶解度大于CuS |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com