
| A. | ①② | B. | ③④ | C. | ①④ | D. | ②④ |
分析 弱电解质是指:在水溶液里部分电离的电解质,电解质分子、电离出的离子共存,据此即可解答.
解答 解:①常温下NaNO2溶液,根据盐类水解的规律,无弱不水解,有弱才水解,越弱越水解,谁强显谁性,如果NaNO2是强酸强碱盐,PH=7,而题干中PH>7,说明NaNO2为强碱弱酸盐,故①正确;
②用HNO2溶液做导电性实验灯泡很暗,溶液的导电性与离子的浓度有关,弱电解质的浓度大时导电实验中灯泡也很亮,没有对比实验,无法说明HNO2是弱电解质,故②错误;
③HNO2与NaCl不能反应,无论亚硝酸是强酸还是弱酸,它们间都不反应,故③错误;
④0.1mol/L HNO2溶液的PH=2.1.如果亚硝酸是强酸,0.1mol/L HNO2溶液的PH应该等于1,而此时PH=2.1,说明电离出的氢离子浓度小,说明HNO2为弱电解质,故④正确;
故选C.
点评 本题考查酸的通性及弱电解质的判断,明确弱电解质的判断方法是利用电离的不完全性或存在电离平衡来分析是解答本题的关键,题目难度不大.


 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 分子数之比为1:1 | B. | 原子数之比为1:1 | C. | 原子数之比为3:2 | D. | 物质的量之比2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:3 | C. | 3:1 | D. | 1:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
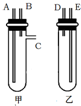 某兴趣小组要进行有关氢气的定量测定实验,为保证氢气不损失,设计用甲、乙两装置及橡胶管完成锌粒和稀硫酸制取氢气的操作.步骤如下:
某兴趣小组要进行有关氢气的定量测定实验,为保证氢气不损失,设计用甲、乙两装置及橡胶管完成锌粒和稀硫酸制取氢气的操作.步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(D)=1mol/(L•s) | B. | v(B)=1mol/(L•min) | C. | v(A)=0.5mol/(L•s) | D. | v(C)=0.8mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol NH3 分子 | B. | NH3和NH4+ 总共1 mol | ||
| C. | NH3•H2O 1 mol | D. | NH3•H2O、NH3、NH4+ 总共1 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com