
| A. | 金刚石>晶体硅>碳化硅 | B. | HI>HBr>HCl>HF | ||
| C. | NaF>NaCl>NaBr | D. | NaCl>Hg>S |
分析 A.原子晶体中半径越小,键长越短,共价键越强,熔点越大;
B.氢化物中分子间存在氢键的熔沸点较高;
C.离子晶体中离子半径越小,电荷越大,熔点越大;
D.离子晶体的熔沸点一般高于分子晶体,Hg常温下为液体.
解答 解:A.原子晶体中半径越小,键长越短,共价键越强,熔点越大,因键长C-C<C-Si<Si-Si,则熔沸点为金刚石>碳化硅>晶体硅,故A错误;
B.氢化物中分子间存在氢键的熔沸点较高,没有氢键时,相对分子质量越大,分子间作用力越强,熔沸点越高,则熔沸点为HF>HI>HBr>HCl,故B错误;
C.因离子半径F-<Cl-<Br-,则熔点为NaF>NaCl>NaBr,故C正确;
D.离子晶体的熔沸点一般高于分子晶体,Hg常温下为液体,所以熔沸点:NaCl>S>Hg,故D错误;
故选C.
点评 本题考查晶体熔点的比较,明确不同类型晶体熔点的比较方法是解答本题的关键,题目难度不大.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 稀释溶液,$\frac{c(HC{O}_{3}^{-})•c(O{H}^{-})}{c(C{O}_{3}^{2-})•c({H}^{+})}$增大 | |
| B. | 通入CO2,或者加入少量氯化铵溶液,溶液pH均减小 | |
| C. | 升高温度,红色变深,平衡常数增大 | |
| D. | 加入NaOH固体,$\frac{c(HCO_3^-)}{{c(CO_3^{2-})}}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO是具有刺激性的红棕色气体 | |
| B. | SO3溶于水生成亚硫酸 | |
| C. | 向品红溶液中通入二氧化硫气体,溶液褪色,加热后溶液又会出现红色 | |
| D. | 氨水中滴入酚酞溶液,颜色变蓝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
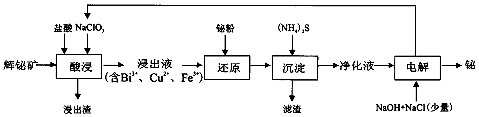
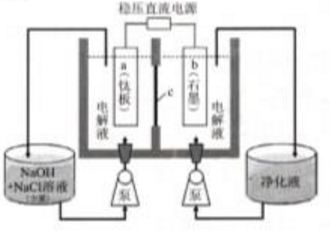
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g D2O和18 g H2O中含有的质子数均为10NA | |
| B. | 50 mL 12 mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| C. | 过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.2NA | |
| D. | 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 反应①生成18mol CO2 | B. | 反应②生成2mol CO2 | ||
| C. | 反应③消耗6mol溴单质 | D. | 反应④脱去2mol水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①③均能发生加成反应 | B. | ②④互为同系物 | ||
| C. | ①②③④均属于烃 | D. | ①②④的一氯代物均只有两种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol CnH2n-2(n≥2)中所含的共用电子对数为(3n+1)NA | |
| B. | 25℃时,1L pH=2 的H2SO4溶液中所含H+数为0.01NA | |
| C. | 标准状况下,22.4 L CH3OH 中含有的共价键数为5NA | |
| D. | 60g的乙酸和葡萄糖混合物充分燃烧消耗3NA个O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com