
| ĪļÖŹ | MgCl2 | Mg£ØOH£©2 | MgCO3 |
| Čܽā¶Č£Øg£© | 54.6 | 0.000 84 | 0.039 |
| A£® | ŅŃÖŖMgCO3µÄKsp=2.14”Į10-5 mol2•L-2£¬ŌņĖłÓŠŗ¬ÓŠ¹ĢĢåMgCO3µÄČÜŅŗÖŠ£¬¶¼ÓŠc£ØMg2+£©=c£ØCO32-£©£¬ĒŅc£ØMg2+£©•c£ØCO32-£©=2.14”Į10-5mol2•L-2 | |
| B£® | ³żČ„“ÖŃĪÖŠŗ¬ÓŠµÄMgCl2ŌÓÖŹ£¬×ī¼Ń³żŌÓŹŌ¼ĮĪŖNa2CO3ČÜŅŗ | |
| C£® | ½«ŹŹĮæµÄ±ķÖŠµÄČżÖÖĪļÖŹ·Ö±šÓė×ćĮæĖ®»ģŗĻ£¬³ä·Ö¼ÓČČ”¢×ĘÉÕ£¬×īÖյĹĢĢå²śĪļĻąĶ¬ | |
| D£® | ÓĆŹÆ»ŅĖ®“¦ĄķĖ®ÖŠµÄMg2+ŗĶHCO3-£¬·¢ÉśµÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖMg2++2HCO3-+Ca2++2OH-ØTCaCO3”ż+MgCO3”ż+2H2O |
·ÖĪö A£®µ±ČÜŅŗÖŠČōŗ¬ÓŠĘäĖüµÄMg2+»ņCO32-£¬ČēĀČ»ÆĆ¾£¬ŌņMg2+ŗĶCO32-µÄÅØ¶Č²»ĻąµČ£»
B£®Ģ¼ĖįĆ¾µÄČܽā¶Č½Ļ“󣬳żŌÓ²»³¹µ×£¬ĒāŃõ»ÆÄĘøüÄŃČÜ£¬ĖłŅŌ×ī¼ŃŹŌ¼ĮĪŖNaOH£»
C£®MgCl2Ė®½ā²śÉśĒāŃõ»ÆĆ¾ŗĶĀČ»ÆĒā£¬ĀČ»ÆĒāŅ×»Ó·¢£¬×īÖյĹĢĢå²śĪļŹĒŃõ»ÆĆ¾£»Mg£ØOH£©2×īÖյĹĢĢå²śĪļŹĒŃõ»ÆĆ¾£¬MgCO3Ė®½ā²śÉśĒāŃõ»ÆĆ¾ŗĶĢ¼Ėį£¬Ģ¼Ėį²»ĪČ¶Ø£¬Ņ×·Ö½ā£¬×īÖյĹĢĢå²śĪļŅ²ŹĒŃõ»ÆĆ¾£»
D£®ÓÉÓŚĒāŃõ»ÆĆ¾±ČĢ¼ĖįĆ¾øüÄŃČÜ£¬Ōņ·“Ӧɜ³ÉµÄŹĒĒāŃõ»ÆĆ¾³Įµķ£®
½ā“š ½ā£ŗA£®ŗ¬ÓŠ¹ĢĢåMgCO3µÄČÜŅŗŹĒ±„ŗĶČÜŅŗ£¬Ö»ŅŖĪĀ¶Č²»±ä£¬c£ØMg2+£©•c£ØCO32-£©¾Ķ²»±ä£¬µČÓŚ2.14”Į10-5mol2•L-2£¬µ«ŹĒČÜŅŗÖŠČōŗ¬ÓŠĘäĖüµÄMg2+»ņCO32-£¬ČēĀČ»ÆĆ¾£¬ŌņMg2+ŗĶCO32-µÄÅØ¶Č²»ĻąµČ£¬¹ŹA“ķĪó£»
B£®Ģ¼ĖįĆ¾µÄČܽā¶Č½Ļ“ó£¬ĒāŃõ»ÆĆ¾µÄČܽā¶Č½ĻŠ”£¬Ōņ³żČ„“ÖŃĪÖŠŗ¬ÓŠµÄMgCl2ŌÓÖŹ£¬×ī¼Ń³żŌÓŹŌ¼ĮĪŖNaOHČÜŅŗ£¬¹ŹB“ķĪó£»
C£®½«ŹŹĮæµÄ±ķÖŠµÄČżÖÖĪļÖŹ·Ö±šÓė×ćĮæĖ®»ģŗĻ£¬³ä·Ö¼ÓČČ”¢×ĘÉÕ£¬MgCl2Ė®½ā²śÉśĒāŃõ»ÆĆ¾ŗĶĀČ»ÆĒā£¬ĀČ»ÆĒāŅ×»Ó·¢£¬ĖłŅŌ×īÖյĹĢĢå²śĪļŹĒMgO£¬Mg£ØOH£©2×īÖյĹĢĢå²śĪļŹĒMgO£¬MgCO3Ė®½ā²śÉśĒāŃõ»ÆĆ¾ŗĶĢ¼Ėį£¬Ģ¼Ėį²»ĪČ¶Ø£¬Ņ×·Ö½ā£¬ĖłŅŌ×īÖյĹĢĢå²śĪļŅ²ŹĒMgO£¬¹ŹCÕżČ·£»
D£®ÓĆŹÆ»ŅĖ®“¦ĄķĖ®ÖŠµÄMg2+ŗĶHCO3-£¬ĒāŃõ»ÆĆ¾øüÄŃČÜ£¬Ōņ·“Ӧɜ³ÉĒāŃõ»ÆĆ¾³Įµķ£¬ÕżČ·µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗMg2++2HCO3-+2Ca2++4OH-ØT2CaCO3”ż+Mg£ØOH£©2”ż+2H2O£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²é½ĻĪŖ×ŪŗĻ£¬Éę¼°ÄŃČÜĪļČܽāĘ½ŗā¼°ĘäÓ¦ÓĆ”¢ĪļÖŹµÄ·ÖĄėÓėĢį“攢Ąė×Ó·½³ĢŹ½ŹéŠ“”¢ŃĪµÄĖ®½āŌĄķµČÖŖŹ¶£¬ĢāÄæÄѶČÖŠµČ£¬Ć÷Č·ČܽāĘ½ŗā¼°ĘäÓ°ĻģŅņĖŲĪŖ½ā“š¹Ų¼ü£¬×¢ŅāÕĘĪÕ³żŌÓŹŌ¼ĮµÄŃ”ÓĆŌŌņ£¬ŹŌĢāÅąŃųĮĖѧɜµÄĮé»īÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
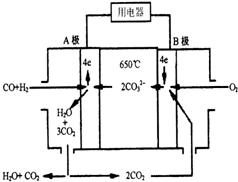 ĻÖÓŠŅ»øöĢ¼ĖįŃĪČ¼ĮĻµē³Ų£¬ŅŌŅ»¶Ø±ČĄżµÄLi2CO3ŗĶNa2CO3µĶČŪ»ģŗĻĪļĪŖµē½āÖŹ£¬²Ł×÷ĪĀ¶ČĪŖ650”ę£¬ŌŚ“ĖĪĀ¶ČĻĀŅŌÄųĪŖ“߻ƼĮ£¬Ö±½ÓŅŌĖ®ĆŗĘų£ØCO”¢H2µÄĢå»ż±ČĪŖ1£ŗ1£©ĪŖČ¼ĮĻ£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£®
ĻÖÓŠŅ»øöĢ¼ĖįŃĪČ¼ĮĻµē³Ų£¬ŅŌŅ»¶Ø±ČĄżµÄLi2CO3ŗĶNa2CO3µĶČŪ»ģŗĻĪļĪŖµē½āÖŹ£¬²Ł×÷ĪĀ¶ČĪŖ650”ę£¬ŌŚ“ĖĪĀ¶ČĻĀŅŌÄųĪŖ“߻ƼĮ£¬Ö±½ÓŅŌĖ®ĆŗĘų£ØCO”¢H2µÄĢå»ż±ČĪŖ1£ŗ1£©ĪŖČ¼ĮĻ£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
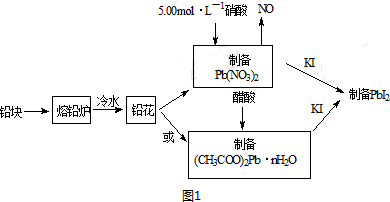
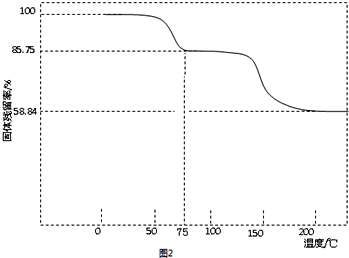
| ŹµŃéÄŚČŻ | ŹµŃé·½·Ø | ŹµŃéĻÖĻó¼°ŌŅņ·ÖĪö |
| ¢ŁµāĄė×ÓÅضČŌö“ó¶ŌĘ½ŗāµÄÓ°Ļģ | Č”PbI2±„ŗĶČÜŅŗÉŁĮæÓŚŅ»Ö§ŹŌ¹ÜÖŠ£¬ŌŁµĪČė¼øµĪNaI±„ŗĶČÜŅŗ | ĻÖĻó£ŗČÜŅŗÖŠc£ØI-£©Ōö“ó£¬Ź¹Q“óÓŚĮĖPbI2µÄKsp |
| ¢ŚĒ¦Ąė×ÓÅØ¶Č¼õŠ”¶ŌĘ½ŗāµÄÓ°Ļģ | Č”PbI2Šü×ĒŅŗÉŁĮæÓŚŅ»Ö§ŹŌ¹ÜÖŠ£¬ŌŁ¼ÓČėÉŁĮæNaCl±„ŗĶČÜŅŗ | ĻÖĻó£ŗ»ĘÉ«»ė×ĒĻūŹ§ ŌŅņ£ŗŠĪ³ÉPbCl42-£¬µ¼ÖĀČÜŅŗÖŠc£ØPb2+£©¼õŠ”£¬Ź¹QcŠ”ÓŚPbI2µÄKsp |
| ¢ŪĒ¦Ąė×ÓŗĶµāĄė×ÓÅØ¶Č¶¼¼õŠ”¶ŌĘ½ŗāµÄÓ°Ļģ | ŌŚPbI2Šü×ĒŅŗÖŠµĪČė¼øµĪFeCl3±„ŗĶČÜŅŗ | ĻÖĻó£ŗ»ĘÉ«»ė×ĒĻūŹ§ Š“³ö·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗPbI2+2Fe3++4Cl-=PbCl42-+2Fe2++I2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
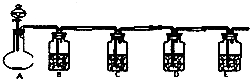 Éč¼ĘŅ»ŹµŃ齫ֻŗ¬ÓŠNa2SO4”¢Na2SO3”¢Na2CO3µÄ°×É«¹ĢĢåÖŠµÄČżÖֳɷּģŃé³öĄ“£®Č”Ņ»¶ØĮæµÄ°×É«¹ĢĢåÓėÉÕĘæAÖŠ£¬Ķعż·ÖŅŗĀ©¶·¼ÓČėŅŗĢåa£¬ČēĶ¼ĖłŹ¾£ŗ
Éč¼ĘŅ»ŹµŃ齫ֻŗ¬ÓŠNa2SO4”¢Na2SO3”¢Na2CO3µÄ°×É«¹ĢĢåÖŠµÄČżÖֳɷּģŃé³öĄ“£®Č”Ņ»¶ØĮæµÄ°×É«¹ĢĢåÓėÉÕĘæAÖŠ£¬Ķعż·ÖŅŗĀ©¶·¼ÓČėŅŗĢåa£¬ČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
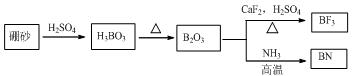
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 25”ꏱ£¬pH=7µÄNH4ClÓėNH3•H2O»ģŗĻČÜŅŗÖŠ£ŗc£ØH+£©=c£ØOH-£©£¼c£ØNH4+£©=c£ØCl-£© | |
| B£® | ½«pH=3µÄ“×ĖįČÜŅŗĻ”ŹĶŗó£¬ČÜŅŗÖŠĖłÓŠĄė×ÓµÄÅØ¶Č¾ł½µµĶ | |
| C£® | ĻņNa2CO3ČÜŅŗÖŠÖšµĪµĪ¼ÓĻ”ŃĪĖįŹ±£¬ČÜŅŗÖŠc£ØHCO3-£©µÄ±ä»ÆĒéæöŹĒĻȱ䊔ŗó±ä“ó | |
| D£® | 0.01 mol•L-1Na2CO3ČÜŅŗÓė0.01 mol•L-1 NaHCO3ČÜŅŗµČĢå»ż»ģŗĻ£ŗ3c£ØCO32-£©+3c£ØHCO3-£©+3c£ØH2CO3£©=2c£ØNa+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 4ÖÖ | B£® | 5ÖÖ | C£® | 6ÖÖ | D£® | 7ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«FeCl2ČÜŅŗŌŚæÕĘųÖŠ¼ÓČČÕōøɲ¢×ĘÉÕ£¬×īÖÕµĆµ½ŗŚÉ«FeO¹ĢĢå | |
| B£® | Ķ¬ÅØ¶ČµÄ°±Ė®£¬NH4Cl”¢£ØNH4£©2SO4ČÜŅŗÖŠĖ®µēĄė³öĒāĄė×ÓÅضČĻąĶ¬ | |
| C£® | Ņ»¶ØÅØ¶ČµÄ°±Ė®ŗĶŃĪĖį»ģŗĻ“ęŌŚ¹ŲĻµ£ŗc£ØNH4+£©+c£ØH+£©=c£ØOH-£©+c£ØCl-£© | |
| D£® | ŹŅĪĀĻĀ£¬0.1mol/LµÄHAČÜŅŗÖŠ$\frac{c£Ø{H}^{+}£©}{c£ØO{H}^{-}£©}$=1010£¬ŌņNaAČÜŅŗĻŌĖįŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com