
 .
.
 .
. .
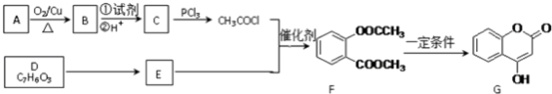
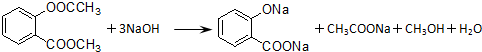
.分析 由CH3COCl结合题中信息(1),可知C为CH3COOH,结合A→B→C的条件可推知B为CH3CHO,A为CH3CH2OH,由F的结构与信息(2),逆推可知E为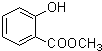 ,结构D的分子式可知,D为
,结构D的分子式可知,D为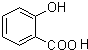 ,据此解答.
,据此解答.
解答 解:由CH3COCl结合题中信息(1),可知C为CH3COOH,结合A→B→C的条件可推知B为CH3CHO,A为CH3CH2OH,由F的结构与信息(2),逆推可知E为 ,结构D的分子式可知,D为
,结构D的分子式可知,D为 .
.
(1)A为CH3CH2OH,名称是乙醇,B为CH3CHO,含有的官能团为醛基,由G的结构简式可知化学式是C9H6O3,
故答案为:乙醇;醛基;C9H6O3;
(2)B→C转化所加的①试剂可能是:银氨溶液或新制Cu(OH)2悬浊液等,D→E的反应类型是酯化反应,
故答案为:银氨溶液或新制Cu(OH)2悬浊液等;酯化反应;
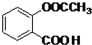
(3)F与足量NaOH溶液反应的化学方程式是: ,
,
故答案为: ;
;
(4)合成路线中生成F的化学方程式是: ,
,
故答案为: ;
;
(5)根据G的结构简式可知,
A.G中有苯环和一个碳碳双键,能够与4mol H2发生加成反应,故A错误;
B.G中没有酚羟基,所以遇FeCl3溶液不能发生显色反应,故B错误;
C.G中有酯基,在NaOH中完全水解产物中含有羧基和酚羟基,与氢氧化钠反应生成羧钠及酚钠,所以分子式为C9H6O4Na2,故C正确,
故选C;
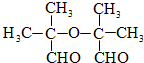
(6)(CH3CO)2O(乙酸酐)与酰氯的化学性质相似.D与乙酸酐反应生成一种常用药物阿司匹林,阿司匹林的结构简式是: ,
,
故答案为: ;
;
(7)E的结构简式为 ,在一定条件下,E与H2加成后生成J(化学式为C8H14O3),则J为
,在一定条件下,E与H2加成后生成J(化学式为C8H14O3),则J为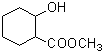 ,同时满足下列条件的J的同分异构体:①不含有环状结构,②含有醛基,③核磁共振氢谱只有两个吸收峰,同分异构体结构简式为:
,同时满足下列条件的J的同分异构体:①不含有环状结构,②含有醛基,③核磁共振氢谱只有两个吸收峰,同分异构体结构简式为: ,
,
故答案为: .
.
点评 本题考查有机物的推断,注意根据转化中有机物的结构、反应条件、反应信息进行推断,需要熟悉掌握官能团的性质与转化,题目难度中等.


科目:高中化学 来源: 题型:选择题
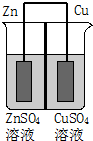 如图为一原电池示意图,在原电池两极之间设有隔膜,离子可以自由通过.则下列说法不正确的是( )
如图为一原电池示意图,在原电池两极之间设有隔膜,离子可以自由通过.则下列说法不正确的是( )| A. | Zn2+通过隔膜从负极区向正极区移动 | |
| B. | 电子由Cu极通过导线流向Zn极 | |
| C. | 一段时间后ZnSO4溶液浓度增大CuSO4溶液浓度减小 | |
| D. | Cu2+与Zn2+物质的量之和保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
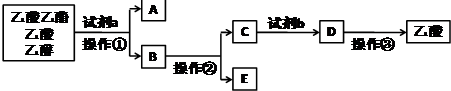
| A. | 操作①用到的玻璃仪器主要有分液漏斗、烧杯 | |
| B. | 工业制备无水E物质的方法是在E中加生石灰后进行操作② | |
| C. | 试剂b可用硫酸 | |
| D. | 操作③用到的仪器和用品主要有漏斗、烧杯、玻璃棒、滤纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
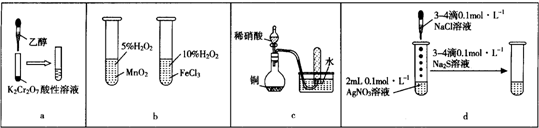
| A. | a图示装置,滴加乙醇试管中橙色溶液变为绿色,乙醇发生消去反应生成乙酸 | |
| B. | b图示装置,右边试管中产生气泡迅速,说明氯化铁的催化效果比二氧化锰好 | |
| C. | c图示装置,根据试管中收集到无色气体,验证铜与稀硝酸的反应产物是NO | |
| D. | d图示装置,试管中先有白色沉淀、后有黑色沉淀,不能验证AgCl的溶解度大于Ag2S |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x+y<z | B. | 平衡向正反应方向移动 | ||
| C. | A的体积分数下降 | D. | B的浓度增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com