
下列化学用语正确的是:( )
A.Cl-的结构示意图: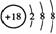
B.光导纤维主要成分的化学式:Si
C.1H2、2H2、3H2互为同位素
D.质子数为53,中子数为78的碘原子:131 53I
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
如图所示是Zn和Cu(稀硫酸)形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是 ( )
| ① Cu为负极,Zn为正极 ② H+向负极移动 ③ 电子的流动方向是:Zn→Cu ④ Cu极上有H2产生 ⑤ 若有1mol电子流经导线,则可产生0.5mol H2气体 ⑥ 正极反应式:Zn-2e-===Zn2+ |
A.①②③ B.③④⑤
C.④⑤⑥ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
把氯气通入浓氨水中,会立即发生下列反应:3Cl2+8NH3·H2O= ==6NH4Cl+N2+8H2O。在标准状况下,把1.12 L Cl2、N2的混合气体(90% Cl2和10% N2,均为体积分数)通过浓氨水,实验测得逸出气体体积为0.672 L(其中有50% Cl2和
==6NH4Cl+N2+8H2O。在标准状况下,把1.12 L Cl2、N2的混合气体(90% Cl2和10% N2,均为体积分数)通过浓氨水,实验测得逸出气体体积为0.672 L(其中有50% Cl2和 50% N2),此反应中被氧化的NH3的质量为 ( )
50% N2),此反应中被氧化的NH3的质量为 ( )
A.3.4 g B.0.34 g
C.1.36 g D.4.48 g
查看答案和解析>>
科目:高中化学 来源: 题型:
正确掌握化学用语是学好化学的基础。下列化学用语中正确的是
A.乙烯的结构简式为CH2CH2 B.乙醇的结构简式为C2H6O
C.丙烷的实验式为 C3H8 D. 羟基的电子式: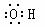
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是
A .钢铁腐蚀时可能发生的反应(正极):2H2O+O2-4e-=4OH-
.钢铁腐蚀时可能发生的反应(正极):2H2O+O2-4e-=4OH-
B.1 L、0.5 mol/L稀硫酸与1 L、1 mol/LNaOH溶液反应放出57.3kJ的热,则其中和热的热化学方程式:H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l);△H= -114.6 kJ/mol
C.碳酸氢钠溶液与足量澄清石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
D.氢氧化铁沉淀可被氢溴酸溶解:2Fe(OH)3+6H++2Br-=2Fe2++Br2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是表示物质组成、结构和变化规律的一种具有国际性、科学性和规范性的书面语言。下列化学用语中,书写错误的是( )
A.硫离子的结构示意图: B.NH4Cl的电子式:
B.NH4Cl的电子式:
C.CO2的电子式:  ············ D.次氯酸的结构式:
············ D.次氯酸的结构式:
查看答案和解析>>
科目:高中化学 来源: 题型:
由黄铜矿(主要成分是CuFeS2) 炼制精铜的工艺流程示意图如下:
炼制精铜的工艺流程示意图如下:
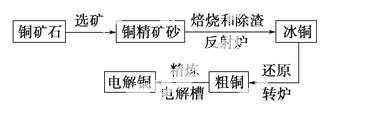
(1)在反射炉中,把铜精矿砂和石英砂混合加热到1 000 ℃左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物。该过程中两个主要反应的化学方程式分别是____________________、__________________________,反射炉内生成 炉渣的主要成分是________;
炉渣的主要成分是________;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1 200 ℃左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是____________;
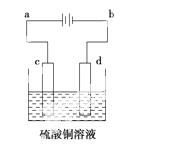
(3)粗铜的电解精炼如右图所示。在粗铜的电解过程中,粗铜板应是图中电极________(填图中的字母);在电极d上发生的电极反应式为____________________________;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。请回答下列问题:
(1)目前,以下“技术”中,可用于“海水淡化”的是___________________________
(填序号)。
①蒸馏法 ②膜分离法(电渗析、反渗透) ③冷冻法 ④离子交换法
(2)海 水晒盐利用的化学原理是____________________________________________;
水晒盐利用的化学原理是____________________________________________;
分离食盐晶体后的母液中含有____________,经过分离、提纯后,可用于_________。
(3)工业上利用电解饱和食盐水可制得重要化工产品,反应的 离子方程式为________________________________________________________________________;
离子方程式为________________________________________________________________________;
电解所用的食盐水需要精制,其原因是_____________________________________
________________________________________________________________________;
精制时所用试剂:盐酸、BaCl2溶液、NaOH溶液、Na2CO3溶液,加入试剂时,Na2CO3溶液必须在加入__________________________________________________________之后加入。
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫的废气同时回收二氧化硫的方法,该方法的流程如下:
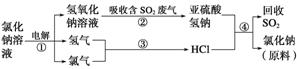
写出反应②、④的化学方程式:_____________________________________________、
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同, b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d中第一电离能最大的是 (填元素符号),e的价层电子轨道示意图为 。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为 ;分子中 既含有极性共价键,又含有非极性共价键的化合物是 (填化学式,写两种)。
既含有极性共价键,又含有非极性共价键的化合物是 (填化学式,写两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是 ;酸根呈三角锥结构的酸是 。(填化学式)
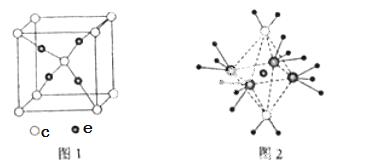
(4)e和c形成的一种离子化合物的晶体结构如图1,则e离子的电荷为 。
(5)这5种元素形成 的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中阴离子为 ,阳离子中存在的化学键类型有 ;该化合物加热时首先失去的组分是
的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中阴离子为 ,阳离子中存在的化学键类型有 ;该化合物加热时首先失去的组分是  ,判断理由是 。
,判断理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com