
(08年上海卷)在2L密闭容器中,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:

(1)写出该反应的平衡常数表达式:K=____。已知:K(300℃)>K(350℃),该反应是________热反应。
(2)右图中表示NO2的变化的曲线是________。用O2表示从0~2s内该反应的平均速率v=_________。
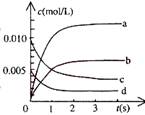
(3)能说明该反应已经达到平衡状态的是______。a、v(NO2)=2v(O2) ;b、容器内压强保持不变
c、v逆(NO)=2v正(O2) d、容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
a、及时分离出NO2气体 ;b、适当升高温度;c、增大O2的浓度 ;d、选择高效的催化剂
答案:(1)K=![]() ;放热。(2)b;1.5×10-3mol/(L?s)。(3)b c。(4)c。
;放热。(2)b;1.5×10-3mol/(L?s)。(3)b c。(4)c。
说明:本题的图象有错误,纵坐标的单位应该是:mol ,0.005应改成0.01,0.010应该为0.020。
解析:该反应的平衡常数表达式:K=![]() ;平衡常数只是温度的函数,平衡常数越大,说明在该温度下反应物转化成生成物的限度越大,反应的转化率越大,K(300℃)>K(350℃),说明低温有利于反应物的转化,该反应的正反应是放热反应。从图上起始浓度看:反应物的浓度随时间变化越来越小,直到平衡时不再减少,图和数据表明,3秒时化学反应达到平衡。曲线c是NO的浓度随时间变化的曲线,曲线d是O2的浓度随时间变化的曲线。生成物的浓度随时间变化越来越大,直到某一时刻,达到平衡时浓度不再增大。本图中有两条从零浓度开始逐渐增大浓度的曲线,根据化学方程式中的计量数关系,NO的浓度减少等于NO2的浓度增加,从图中变化幅度看,曲线b的浓度变化符合计量数关系,所以曲线b是表示NO2的浓度随时间变化的曲线。用NO表示从0~2s内该反应的平均速率v(NO)=
;平衡常数只是温度的函数,平衡常数越大,说明在该温度下反应物转化成生成物的限度越大,反应的转化率越大,K(300℃)>K(350℃),说明低温有利于反应物的转化,该反应的正反应是放热反应。从图上起始浓度看:反应物的浓度随时间变化越来越小,直到平衡时不再减少,图和数据表明,3秒时化学反应达到平衡。曲线c是NO的浓度随时间变化的曲线,曲线d是O2的浓度随时间变化的曲线。生成物的浓度随时间变化越来越大,直到某一时刻,达到平衡时浓度不再增大。本图中有两条从零浓度开始逐渐增大浓度的曲线,根据化学方程式中的计量数关系,NO的浓度减少等于NO2的浓度增加,从图中变化幅度看,曲线b的浓度变化符合计量数关系,所以曲线b是表示NO2的浓度随时间变化的曲线。用NO表示从0~2s内该反应的平均速率v(NO)=![]() =
=![]() =3*10-3 mol?L-1?s-1 ,化学反应速率之比等于计量数之比,用O2表示从0~2s内该反应的平均速率v(O2)=
=3*10-3 mol?L-1?s-1 ,化学反应速率之比等于计量数之比,用O2表示从0~2s内该反应的平均速率v(O2)=![]() v(NO)=1.5*10-3 mol?L-1?s-1 。一定条件下的可逆反应,当正逆反应速率相等时,化学反应达到平衡状态,其特征是各物质的浓度不再发生改变,对于反应强后气体体积不等的可逆反应,在密闭容器中,由于浓度不变,物质的量也不再改变,压强也不再改变,b c正确。化学反应速率之比等于计量数之比,a判断无论可逆反应达到平衡与否,都成立,不是平衡特有的条件。d判断:化学反应遵循质量守恒定律,反应前后的质量不发生改变,密闭容器体积不变,所以密度始终不发生改变,它不是平衡判断的标志。a、及时分离出NO2气体平衡向正反应方向移动了,但是随着反应物浓度的减小,反应速率也减小了。b、适当升高温度,虽然反应速率提高了,由于正反应是放热反应,不利于平衡的正向移动;c、增大O2的浓度,O2是反应物,增大反应物浓度平衡向正反应方向移动,增大浓度化学反应速率增大,符合题意;d、选择高效的催化剂,只能增大化学反应速率,平衡不会发生移动。
v(NO)=1.5*10-3 mol?L-1?s-1 。一定条件下的可逆反应,当正逆反应速率相等时,化学反应达到平衡状态,其特征是各物质的浓度不再发生改变,对于反应强后气体体积不等的可逆反应,在密闭容器中,由于浓度不变,物质的量也不再改变,压强也不再改变,b c正确。化学反应速率之比等于计量数之比,a判断无论可逆反应达到平衡与否,都成立,不是平衡特有的条件。d判断:化学反应遵循质量守恒定律,反应前后的质量不发生改变,密闭容器体积不变,所以密度始终不发生改变,它不是平衡判断的标志。a、及时分离出NO2气体平衡向正反应方向移动了,但是随着反应物浓度的减小,反应速率也减小了。b、适当升高温度,虽然反应速率提高了,由于正反应是放热反应,不利于平衡的正向移动;c、增大O2的浓度,O2是反应物,增大反应物浓度平衡向正反应方向移动,增大浓度化学反应速率增大,符合题意;d、选择高效的催化剂,只能增大化学反应速率,平衡不会发生移动。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
![]()
实验序号 | 甲针筒内物质 | 乙针筒内物质 | 甲针筒的现象 |
1 | 10mLFeSO4溶液 | 10mLNH3 | 生成白色沉淀,后变色 |
2 | 20mLH2S | 10mLSO2 |
|
3 | 30mLNO2(主要) | 10mLH2O(l) | 剩有无色气体,活塞自动向内压缩 |
4 | 15molCl2 | 40mLNH3 |
|
(1)实验1中,沉淀最终变为________色,写出沉淀变色的化学方程式________________________。
(2)实验2甲针筒内的现象是:有___________生成,活塞________移动(填向外、向内、不)。反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入___________溶液中。
(3)实验3中,甲中的3mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是_______,写出NO2与H2O反应的化学方程式为_______________________________。
(4)实验4中,已知:3Cl2+2NH3→N2+6HCl。甲针筒出活塞有移动,针筒内有白烟产生外,气体的颜色变为____________。最后针筒内剩余气体的体积约为________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
(08年上海卷)(B类卷)某实验小组用下列装置进行乙醇催化氧化的实验。
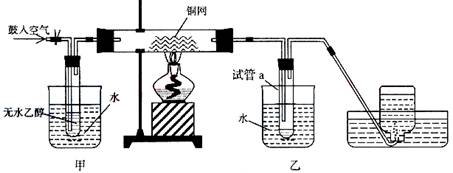
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式______________。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇氧化反应是______反应。
(2)甲和乙两个水浴作用不相同。甲的作用是_____________;乙的作用是___________________。
(3)反应进行一段时间后,干燥管a中能收集到不同的物质,它们是___________。集气瓶中收集到的气体的主要成分是____________。
(4)若试管a中收集到的液体用紫色石蕊试纸,试纸显红色,说明液体中还有____________。要除去该物质,可先在混合液中加入_________(填写字母)。a、氯化钠溶液;b、苯;c、碳酸氢钠溶液 d、四氯化碳;然后再通过___________(填实验操作名称)即可除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
(08年上海卷)已知: 物质A在体内脱氢酶的作用下会氧化为有害物质GHB。下图是关于物质A的一种制备方法及由A引发的一系列化学反应。
![]()

请回答下列问题:
(1)写出反应类型:反应①____________,反应②____________。
(2)写出化合物B的结构简式_____________________________。
(3)写出反应②的化学方程式____________________________。
(4)写出反应④的化学方程式____________________________。
(5)反应④中除生成E外,还可能存在一种副产物(含![]() 结构),它的结构简式为________________。
结构),它的结构简式为________________。
(6)与化合物E互为同分异构体的物质不可能为________(填写字母)。
a、醇 b、醛 c、羧酸 d、酚
查看答案和解析>>
科目:高中化学 来源: 题型:
(08年上海卷)等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实验组别可能是 ( )
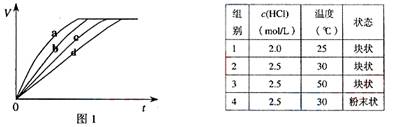
A.4-3-2-1 B.1-2-3-4 C.3-4-2-1 D.1-2-4-3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com