
| A. | 甲烷 | B. | 乙烯 | C. | 二氧化硫 | D. | 碘化钾 |
分析 根据高锰酸钾具有强氧化性,一般来说,具有还原性的无机物,含有碳碳双键、醛基的物质以及一些醇类、酚类、苯的同系物等可被高锰酸钾氧化,以此解答该题.
解答 解:A.甲烷性质稳定,不能够被酸性高锰酸钾溶液氧化,故A选;
B.乙烯分子中含有碳碳双键,能够被酸性高锰酸钾溶液氧化,从而使酸性高锰酸钾溶液褪色,故B不选;
C.二氧化硫具有还原性,能使酸性高锰酸钾溶液褪色,故C不选;
D.碘化钾具有还原性,能使酸性高锰酸钾溶液褪色,故D不选;
故选A.
点评 本题考查了常见有机物的结构与性质,题目难度不大,注意掌握常见有机物的结构及具有的化学性质,明确酸性高锰酸钾溶液褪色的原理是解答本题的关键.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
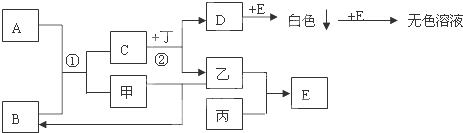
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何金属元素与非金属元素之间的化合 | |
| B. | 任意两种元素之间的化合 | |
| C. | 典型活泼金属和典型活泼非金属之间的化合 | |
| D. | 两种非金属元素之间的化合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中有一个或多个苯环的化合物 | |
| B. | 分子组成满足通式CnH2n-6(n≥6)的化合物 | |
| C. | 分子中含有苯环的烃 | |
| D. | 苯及苯的同系物的总称 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和丙烷 | B. | 甲烷和丙烷 | C. | 甲烷和丙烯 | D. | 乙烯和丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气和天然气的进人量都减少 | |
| B. | 减小天然气的进人童或增大空气的进入量 | |
| C. | 空气和天然气的进人童都增大 | |
| D. | 增大天然气的进人量或减小空气的进入量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
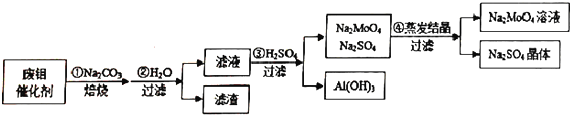
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 粒子符号 | 相对分子质量 | 每个粒子的质量(g/个) | 1mol物质含有的粒子数(个) | 1摩尔物质质量(g) |
| C | 12 | 1.993×10-23 | 6.02×1023 | |
| Fe | 56 | 9.302×10-23 | 6.02×1023 | |
| H2O | 18 | 1.628×10-22 | 6.02×1023 | |
| H2SO4 | 98 | 2.990×10-23 | 6.02×1023 | |
| Na+ | 23 | 3.821×10-23 | 6.02×1023 | |
| OH- | 17 | 2.824×10-23 | 6.02×1023 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com