
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | L2+与R2-的核外电子数相等 | B. | 单质与稀盐酸反应的速率为L<Q | ||
| C. | M与T形成的化合物具有两性 | D. | 氢化物的沸点为H2T<H2R |
分析 短周期元素中,R和T的化合价都有-2价,处于ⅥA族,R的最高价为+6价,T无正价,且R的原子半径较大,则R为S元素,T为O元素;L和Q的化合价都为+2价,处于ⅡA族,且L的原子半径大于Q的,则Q为Be,L为Mg;M的化合价为+3价,为周期表第ⅢA族元素,而M原子半径大于硫、小于Mg,则M为Al.
A.核外电子数=质子数-离子带的电荷;
B.金属性越强,与酸反应越剧烈;
C.氧化铝能与酸反应生成相应的盐与水,与碱反应生成相应的盐与水;
D.分子之间形成氢键,增大物质的沸点.
解答 解:短周期元素中,R和T的化合价都有-2价,处于ⅥA族,R的最高价为+6价,T无正价,且R的原子半径较大,则R为S元素,T为O元素;L和Q的化合价都为+2价,处于ⅡA族,且L的原子半径大于Q的,则Q为Be,L为Mg;M的化合价为+3价,为周期表第ⅢA族元素,而M原子半径大于硫、小于Mg,则M为Al.
A.Mg2+核外有10个电子,S2-核外有18个电子,二者核外电子数不同,故A错误;
B.金属性Mg>Be,则Mg与酸反应越剧烈,则相同条件下单质与稀盐酸反应速率为Q<L,故B错误;
C..M与T形成的化合物是氧化铝,能与酸反应生成相应的盐与水,与碱反应生成相应的盐与水,氧化铝是两性氧化物,故C正确;
D.水分子之间形成氢键,沸点高于硫化氢的,故D错误.
故选:C.
点评 本题考查结构性质位置关系应用,关键是根据原子半径及化合价来推断元素,注意对元素周期律的理解,熟悉元素及其单质、化合物的性质.


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA | |
| B. | 由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 | |
| C. | 1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA个 | |
| D. | 60g二氧化硅中含有的共价键数为2NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
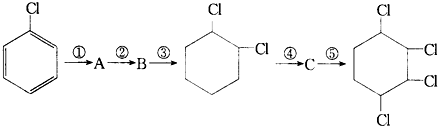
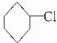 B
B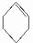
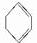 .
.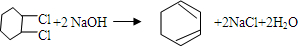 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl>NH3>HI | B. | HI>HCl>NH3 | C. | HCl>HI>NH3 | D. | NH3>HI>HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
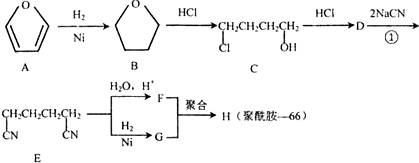
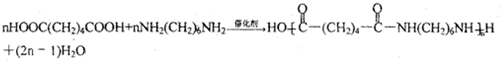 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 海水密度(g/mL) | CaSO4 | NaCl | MgCl2 | Mg SO4 | NaBr |
| 1.20 | 0.91 | ||||
| 1.21 | 0.05 | 3.26 | 0.004 | 0.008 | |
| 1.22 | 0.015 | 9.65 | 0.01 | 0.04 | |
| 1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
| 1.31 | 1.40 | 0.54 | 0.03 | 0.06 |
| A. | CaSO4 | B. | MgSO4 | C. | NaCl | D. | MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
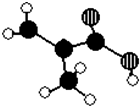 某化工厂生产的某产品A只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).
某化工厂生产的某产品A只含C、H、O三种元素,其分子模型如图所示(图中球与球之间的连线代表化学键,如单键、双键等).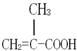 ,用1H核磁共振谱可以证明该化合物的核磁共振氢谱中有3个吸收峰.
,用1H核磁共振谱可以证明该化合物的核磁共振氢谱中有3个吸收峰.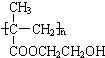 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com