
| A.强电解质的饱和溶液一定是浓溶液 |
| B.凡是能导电的物质都是电解质 |
| C.氯气不是电解质,所以氯水不导电 |
| D.硫酸是强电解质 |
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.①②③④⑤ | B.①②③⑤ | C.②③④ | D.④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
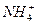 )=2.0×10-6 mol·L-1、C(Cl-)=3.5×10-6 mol·L-1、C(
)=2.0×10-6 mol·L-1、C(Cl-)=3.5×10-6 mol·L-1、C(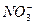 )=4.5×10-6 mol·L-1、C(
)=4.5×10-6 mol·L-1、C(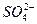 )=5.0×10-6 mol·L-1,则此雨水的pH约为( )
)=5.0×10-6 mol·L-1,则此雨水的pH约为( )| A.3 | B.4 | C.5 | D.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.NaHS溶于水:NaHS Na++HS- Na++HS- |
B.(NH4)2SO4溶于水:(NH4)2SO4 2 2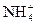 + +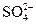 |
C.氢氟酸溶液:HF+H2O H3O++F- H3O++F- |
D.NaHCO3溶于水:NaHCO3 Na++H++ Na++H++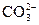 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
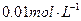 氢氧化钠的PH=11水的离子积常数KW是多少?
氢氧化钠的PH=11水的离子积常数KW是多少?查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H+ Ba2+ Mg2+ Cl- |
| B.Cl- CO32- Cu2+ Fe2+ |
| C.NO3- K+ H+ SO42- |
| D.OH- Na+ NO3-Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.2mol/L醋酸溶液与 0.1mol/L醋酸溶液中c(H+)之比 |
| B.(NH4)2SO4溶液中c(NH4+)和c(SO42-)的物质的量浓度之比 |
| C.pH= 2的盐酸和pH=12的Ba(OH)2溶液中溶质的物质的量浓度之比 |
| D.0.2 mol/LCH3COONa溶液与 0.1mol/L Na2CO3溶液中c(CH3COO-)与c(CO32-)之比 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com