



科目:高中化学 来源: 题型:
| A、NH4Cl |
| B、NaOH固体 |
| C、MgCl2固体 |
| D、NaCl固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.7 |
| Cu2+ | 4.9 | 6.7 |
| Al3+ | 3.0 | 4.4 |
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:


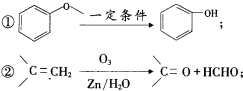
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
| B、Ksp?Kw=Kh | ||
| C、Ksp?Kh=(Kw)3 | ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、难溶电解质的Ksp越大,其溶解度一定越大 |
| B、活化能的作用在于使反应物活化,从而启动反应或改变反应速率 |
| C、水的离子积常数就是水的电离平衡常数 |
| D、同为酸式盐,NaHS溶液显碱性而Na2HPO4溶液显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、-(2b+2c-a)kJ?mol-1 |
| B、-(a-2b-2c)kJ?mol-1 |
| C、-(b+c-a)kJ?mol-1 |
| D、-(a-b-c)kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com