
| A����Һ | B������ | AB�IJ��� |
�� | 7. | 2. | 6. |
�� | 4. | 5.00 | 6. |
�� | ag | bg | 4. |
����
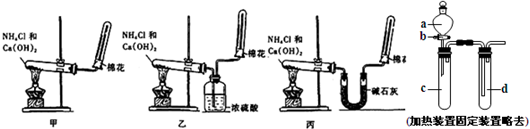
(1)A+B![]() AB�ķ�Ӧ�У�A��B��AB���������ȣ�
AB�ķ�Ӧ�У�A��B��AB���������ȣ�
(2)��ͬѧ��ʵ���У�a��b��ֵ�ֱ�Ϊ���١�
(1)2��1��3
(2)a=2.96��b=6.04(A����);a=7.52��b=1.48(B����)
��ʾ��(1)�ɼ�֪��������������2��1��3�����ҵ�����֪����A����ʱ����������Ϊ1��5��6����B����ʱ������������2��1��3�����ס��ҽ���������ɵ�����������ӦΪ2��1��3��
(2)����(1)�Ľ���ɼ����������4.



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Һ | B������ | AB�IJ��� |
�� | 7.00 g | 2.00 g | 6.00 g |
�� | 4.00 g | 5.00 | 6.00 g |
�� | a g | b g | 4.44 g |
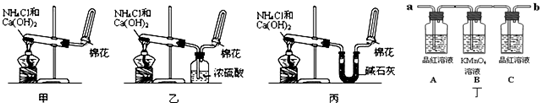
����1��A+B![]() AB�ķ�Ӧ�У��μӷ�Ӧ�����������ȣ�
AB�ķ�Ӧ�У��μӷ�Ӧ�����������ȣ�
���ɼ�ͬѧʵ��õ������ߵ������Ⱥ�����ͬѧ�õ������ߵ������ȣ����ɴ���μӷ�Ӧ�����ߵ������ȡ�
��2����ͬѧ��ʵ���У�a��b��ֵ�ֱ�Ϊ���١�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com