
【题目】下列关于化学学习和研究的说法错误的是( )
A.化学模型有助于解释一些化学现象B.质量守恒定律是大量实验事实的总结
C.化学家提出的假设都能被实验证明D.化学基本原理的应用是有一定条件的
科目:高中化学 来源: 题型:
【题目】(1)向AlCl3溶液中,滴加少量NaOH溶液,现象是________________________
继续滴加NaOH溶液至过量,现象是_______________。
(2)钠与水反应的离子方程式为_______________,该反应中氧化剂是_______________,产生1mol H2时,转移电子的物质的量为_______________mol。
(3)经常有人因误食亚硝酸钠(NaNO2)而中毒。原因是NaNO2像食盐一样既有咸味,又有很强毒性。已知亚硝酸钠能发生如下反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O
①该反应的氧化剂是_______,被氧化的是_________元素。
②若此反应中电子转移数目为0.5mol,则被氧化的还原剂的物质的量为___________。
【答案】 产生白色沉淀 白色沉淀消失 2Na + 2H2O ![]() 2Na++ 2OH- + H2↑ 水或H2O 2 NaNO2 碘(或I) 0.5 mol
2Na++ 2OH- + H2↑ 水或H2O 2 NaNO2 碘(或I) 0.5 mol
【解析】(1)向AlCl3溶液中,滴加少量NaOH溶液,发生反应AlCl3+3NaOH═Al(OH)3↓+3NaCl,现象是产生白色沉淀;继续滴加NaOH溶液至过量,发生反应Al(OH)3+NaOH═NaAlO2+2H2O,现象是白色沉淀消失;(2)钠与水反应生成氢氧化钠与氢气,反应离子方程式为:2Na + 2H2O ![]() 2Na++ 2OH- + H2↑,反应中水中H元素化合价由+1价降低为0价,水是氧化剂,生成1molH2时转移电子的物质的量为1mol×2=2mol;(3)①反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O中,元素化合价的变化分别如下:氮元素:NaNO2 →NO,由+3价→+2价,得电子,所以NaNO2是氧化剂;碘元素,HI→I2,由-1价→0价,失电子,被氧化的是碘元素;②根据反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O可知,若此反应中电子转移数目为0.5mol,则被氧化的还原剂的物质的量为0.5 mol。
2Na++ 2OH- + H2↑,反应中水中H元素化合价由+1价降低为0价,水是氧化剂,生成1molH2时转移电子的物质的量为1mol×2=2mol;(3)①反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O中,元素化合价的变化分别如下:氮元素:NaNO2 →NO,由+3价→+2价,得电子,所以NaNO2是氧化剂;碘元素,HI→I2,由-1价→0价,失电子,被氧化的是碘元素;②根据反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O可知,若此反应中电子转移数目为0.5mol,则被氧化的还原剂的物质的量为0.5 mol。
【题型】综合题
【结束】
19
【题目】国际化学年的中国宣传口号是“化学-----我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”道理。请填空:
(1)①若金属钠等活泼金属着火时,应该_______________用来灭火。
②经火焰灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)的元素是。_______________
③胃舒平(含有氢氧化铝)可治疗胃酸过多,其反应的离子反应方程式为:_______________。
④明矾能净水,其电离方程式是_______________。
(2)过氧化钠作潜艇供氧剂时发生的化学反应方程式是_____________。
(3)加热Al片的实验现象是_________________,原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一定体积CH4、C2H6、C3H8组成的混合气体,是同温同压下H2密度的15倍。则混合气体中CH4、C2H6、C3H8、的体积比不可能是: ( )
A. 2∶1∶2 B. 2∶3∶1 C. 1∶4∶1 D. 5∶3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料.粗食盐常含有少量Ca2+、Mg2+、SO42﹣等杂质离子,实验室提纯NaCl的流程如图: 
提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液
(1)从上述提供的试剂中选出适当的试剂除去溶液I中的Ca2+、Mg2+、SO42﹣离子,滴加顺序依次为、、(只填化学式).
(2)操作Ⅲ的名称是 , 所需用到的仪器主要有铁架台、酒精灯、铁圈、(填仪器名称).
(3)加盐酸的目的是(用离子方程式表示)、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国政府为了消除碘缺乏病,规定在食盐中必须加人适量的碘酸。检验食盐中是否加碘,可利用如下反应:KIO3+ 5 KI+ 3H2SO4═3K2SO4+ 3I2 + 3H2O
(1)该反应中氧化剂和还原剂的物质的量之比为__________;
(2)用双线桥表示电子转移方向和数目___________________。
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为_________;
(4)若要提取生成的碘,所用的萃取剂可以是________(填序号)。
①水 ②酒精 ③淀粉溶液 ④四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+mY(g)3Z(g),平衡时,X,Y,Z的体积分数分别为30%、60%、10%,在此平衡体系中加入1molZ(g),再将达到平衡后,X,Y,Z的体积分数不变.下列叙述不正确的是( )
A.m=2
B.两次平衡的平衡常数相同
C.X与Y的平衡转化率之比为1:1
D.第二次平衡时,Z的浓度为0.4molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业产生的废气COX、NOX、SOX 对环境有害,若能合理的利用吸收,可以减少污染,变废为宝.
(1)有一种用CO2生产甲醇燃料的方法:CO2+3H2CH3OH+H2O 已知:CO2(g)+3H2(g)═CH3OH(g)+H2O(l)△H=﹣akJmol﹣1;
2H2(g)+O2(g)═2H2O(l)△H=﹣b kJmol﹣1;
CH3OH(g)═CH3OH(l)△H=﹣c kJmol﹣1;
则表示CH3OH(l)燃烧热的热化学方程式为: .
(2)光气(COCl2)是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过Cl2(g)+CO(g)COCl2(g)制备.图1为此反应的反应速率随温度变化的曲线,图2为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线.回答下列问题: 
①0~6min内,反应的平均速率v(Cl2)=;
②10min改变的条件是 , 该反应平衡常数变化的趋势是(填“增大”、“减小”或“不变”).
(3)利用氨水可以将SO2和NO2吸收,原理如图3所示:NO2被吸收的离子方程式是 . 
(4)用粗硅作原料,熔融盐电解法制取硅烷原理如图4,判断B为电源的极,电解时阳极的电极反应式为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用溶解、过滤、结晶的方法来分离的一组物质是
A. NaCl和Na2SO4 B. CuO和KCl C. BaSO4和CaCO3 D. NaNO3和NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用实验室制法制备NH3并用制得的氨气做一些性质实验。设计如下的装置(图中铁夹等夹持装置已略去),进行有关实验。
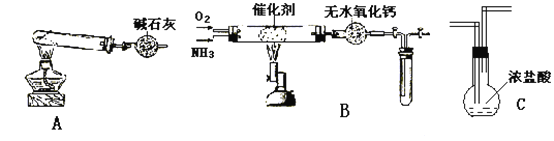
(1)装置A制取纯净、干燥的氨气,大试管内发生的化学方程式:_______________________,A中装碱石灰的仪器名叫________________ ,碱石灰的作用____________________,收集氨气应用____________________法,检验氨气是否集满的方法及现象是_______________________。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式:_________________________________________________。
② B装置右侧试管内气体变为红棕色,该反应的化学方程式:____________________。
(3)若将氨气通入C中现象为_____________,反应的方程式:_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com